

 ;
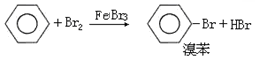
;分析 (1)苯和液溴在催化剂条件下能发生取代反应生成溴苯;
(2)溴苯中的溴易挥发,挥发的溴影响HBr的检验,应除去,再结合非极性分子的溶质易溶于非极性分子的溶剂,据此分析苯的作用;
(3)该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银;
(4)导气管插入水中,三颈烧瓶中压强减小易产物倒吸;
(5)溴苯是有机物,不溶于氢氧化钠溶于苯,溴单质能溶解于溴苯,且密度大于氢氧化钠溶液.
解答 解:(1)苯和液溴在催化剂条件下能发生取代反应生成溴苯,反应方程式为 ;
;
故答案为: ;
;
(2)溴苯中的溴易挥发,根据相似相溶原理选择四氯化碳或苯溶解挥发出的溴,防止干扰HBr的检验;
故答案为:CCl4或苯;除去HBr中混有的溴蒸气;
(3)该反应中有溴化氢生成,溴化氢溶于水得到氢溴酸,氢溴酸是酸性物质,能使石蕊试液变红色;氢溴酸能和硝酸银反应生成淡黄色沉淀溴化银,所以观察E和F两试管,看到的现象是E管中变红,E管中出现浅黄色沉淀,证明生成了溴化氢证明是取代反应;
故答案为:E管中石蕊试液变红,F试管中出现浅黄色沉淀;
(4)打开G活塞,关闭C活塞,HBr易溶解于水,导致三颈烧瓶中压强减小,产物倒吸现象;故答案为:水倒吸至三颈烧瓶中;
(5)实验结束后,得到粗溴苯中含有溴单质和苯,可以先水洗、再碱洗并分液,最后用干燥剂干燥后再蒸馏即可得到溴苯,正确的操作顺序是:bdeca或edbca;
故答案为:bdeca或edbca.
点评 本题考查了苯的取代反应实验,考查的知识点有反应方程式的书写、产物的判断、蒸汽的成分及性质,综合性较强,难度较大,注意苯能和液溴发生取代反应,和溴水不反应.


科目:高中化学 来源: 题型:选择题

| A. | 图一:引发铝热反应的操作是点燃镁条 | |
| B. | 图二:可用于化学反应速率的测定 | |
| C. | 图三:滴加K3[Fe(CN)6]溶液,产生特征蓝色沉淀 | |
| D. | 图四:酸式滴定管注入Na2CO3溶液之前应检查是否漏液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2含量增加会导致温室效应 | |
| B. | 为减少木材的使用,使用聚氯乙烯生产包装盒 | |
| C. | 装修材料中的甲醛、芳香烃等会造成污染 | |
| D. | 天然气代替煤作燃料可减少环境污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃料不完全燃烧排放的CO是大气污染物之一 | |
| B. | 采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,可提高空气质量 | |
| C. | 将已成熟的水果放入未成熟的水果中并密封,可加速水果成熟 | |
| D. | 医用消毒酒精中乙醇的浓度(体积分数)为95% |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .水源中的NO3-对人类健康会产生危害.为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理.
.水源中的NO3-对人类健康会产生危害.为了降低水源中NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为10Al+6NO3-+4OH-=10AlO2-+3N2↑+2H2O,此方法的缺点是处理后的水中生成了A1O3-,仍然可能对人类健康产生危害,还需要对该饮用水进行一系列后续处理.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 我国科学家屠呦呦因发现青蒿素治疗疟疾新疗法而获得2015年诺贝尔生理学或医学奖,已知青蒿素的结构简式如图.下列说法不正确的是( )
我国科学家屠呦呦因发现青蒿素治疗疟疾新疗法而获得2015年诺贝尔生理学或医学奖,已知青蒿素的结构简式如图.下列说法不正确的是( )| A. | 青蒿素可能具有强氧化性,具有杀菌消毒作用 | |
| B. | 青蒿素难溶于水,能溶于NaOH溶液 | |
| C. | 青蒿素分子中含有碳氧双键,但不能发生加成反应 | |
| D. | 青蒿素与纤维素一样,都属于有机高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17 g H2O2与17 g H2S所含的电子数均为9NA | |
| B. | 0.3 mol NO2与水反应,生成H+数目为0.3NA | |
| C. | 0.1 mol Cl2通入适量水中,转移电子数为0.2NA | |
| D. | 2 L pH=3的醋酸与足量的锌反应,产生H2分子数为10-3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | O-16可以表示为:${\;}_{16}^{32}$O | B. | 对硝基甲苯的结构简式: | ||
| C. | 羟基的电子式: | D. | 二氧化碳分子的比例模型: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com