
 ="2." 500×10-3 mol
="2." 500×10-3 mol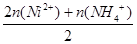 =
=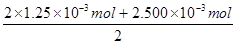 ="2." 500×10-3mol
="2." 500×10-3mol 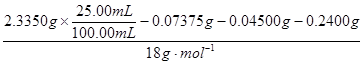 ="1." 250×10-2 mol
="1." 250×10-2 mol 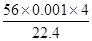 =0.01mol
=0.01mol

 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源:不详 题型:单选题
| A.足量Fe与1 mol Cl2燃烧反应时,转移的电子数为3 NA |
| B.1 mol NO2与足量H2O反应,转移的电子数为NA |
| C.常温常压下,9.2g的NO2和N2O4混合气体中含有的氮原子数为0.2 NA |
| D.高温、催化剂作用,0.4 mol SO2与足量氧气反应生成的SO3分子数为0.4 NA |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0L | B.8.96L | C.15.68 L | D.26.88L |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.22 | B.44 | C.28.25 | D.88 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.n>1 | B.n=1 | C.0.5≤n<1 | D.n<0.5 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.0.16mol | B.0.8 mol | C.0.4mol | D.0.2mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.乙酸乙脂的化学式为C4H8O2 |
| B.结构简式为CH3CH(CH3)2的有机物叫异丁烷 |
| C.HF叫氢氟酸 |
D.CO2的电子式为  |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.1:1 | B.1:3 | C.2:1 | D.3:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com