
下图是某学校实验室买回的硫酸试剂标签的部分内容。判断下列说法正确的是( )
| 硫酸化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g·cm-3 质量分数:98% |
A.该硫酸的浓度为9.2 mol·L-1
B.配制200 mL 4.6 mol·L-1的稀H2SO4需该H2SO450 mL
C.该硫酸与等体积水混合质量分数变为49%
D.取该硫酸100 mL,则浓度变为原来的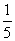
科目:高中化学 来源: 题型:
海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,最后电解得到金属镁。
(1)加碱沉淀镁离子时,生成的Mg(OH)2在分散系中处于沉淀溶解平衡,其溶度积常数表达式Ksp= 。
(2)MgCl2溶液显酸性,其水解的离子方程式为 。
(3)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有 。
a.MgO b.NaOH c.Mg(OH)2 d.MgSO4
(4)若在空气中加热MgCl2·6H2O,可水解生成Mg(OH)Cl,写出相关的化学方程式 。所以,为了抑制MgCl2·6H2O在加热时水解,可在干燥的
气流中加热,可得到无水氯化镁。
(5)用惰性电极电解熔融的MgCl2,阳极的电极反应式为: ;
如果电解MgCl2溶液,阴极的电极反应式为: 。
查看答案和解析>>
科目:高中化学 来源: 题型:
同一状态下,20 mL A2气体与30 mL B2气体恰好完全反应生成20 mL某气体X,则X的化学式为( )
A.A2B3 B.AB2
C.AB3 D.A3B2
查看答案和解析>>
科目:高中化学 来源: 题型:
物质的量浓度相同的NaNO3、Mg(NO3)2、Al(NO3)3三种溶液,取三种溶液的体积比为3:2:1时,三种溶液中c(NO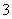 ) 之比为( )
) 之比为( )
A.1:1:1 B.1:2:3
C.3:2:1 D.3:4:3
查看答案和解析>>
科目:高中化学 来源: 题型:
有一包白色固体,可能含有K2CO3、Na2SO4、KCl、CuSO4中的一种或几种。为探究其成分,张华同学进行了如下实验:
(1)取少量白色固体于试管中加水溶解,得到无色澄清溶液,因此他认为肯定有一种物质不存在,这种物质的化学式为__________,推断的依据是________________________________________ ________________________________。
(2)接着又向试管中加入稍过量的BaCl2溶液和稀HNO3,观察到先有白色沉淀生成,而后白色沉淀部分溶解并产生无色气泡。因此他认为肯定存在两种物质,它们的名称是________________________________________________________________________________,推断的依据是________________________ __________。
(3)将所得到的混合物过滤,取滤液少量于另一洁净的试管中,加入稍过量的AgNO3溶液和稀HNO3,结果也得到了白色沉淀。因此他认为原白色固体中肯定存在KCl。你认为他的结论________(填“对”或“不对”),理由是________________________________________________________________________________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中,氧化剂和还原剂为同一种物质的是( )
A.2Na+2H2O===2NaOH+H2↑
B.MnO2+4HCl(浓)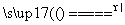 MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
C.Na2CO3+CO2+H2O===2NaHCO3
D.2Na2O2+2CO2===2Na2CO3+O2
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室也可用KMnO4固体和浓盐酸反应制氯气,反应方程式如下:2KMnO4+16HCl(浓)===2KCl+2MnCl2+8H2O+5Cl2↑。回答下列问题:
(1)该反应中氧化剂是__________,还原产物是____________。
(2)若参加反应的高锰酸钾为7.9 g,被氧化的HCl的物质的量是多少?把生成的氯气全部通入足量氢氧化钠溶液中,生成次氯酸钠多少克?
查看答案和解析>>
科目:高中化学 来源: 题型:
在Fe2(SO4)3、CuSO4和稀H2SO4的混合液中加入Fe粉,反应结束后,所剩余的固体滤出后能被磁铁吸引,则反应后溶液中存在较多的阳离子是
A.Fe3+ B.Cu2+
C.Fe2+ D.H+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com