
【题目】依据氧化还原反应:2Ag+(aq)+Cu(s)=Cu2+(aq)+2Ag(s)设计的原电池如图所示。请回答下列问题:

(1)电极X的材料是 (化学式);电解质溶液Y是 ;
(2)银电极为电池的 极,发生的电极反应为 ;X电极上发生的电极反应为 ;
(3)外电路中的电子是从 电极流向 电极。
【答案】(10分)
(1)Cu (1分);AgNO3溶液 (2分)。
(2)正 (1分), Ag++e- = Ag (2分); Cu-2e- = Cu2+ (2分)。
(3) 负(Cu) (1分);正(Ag) (1分)。
【解析】
试题分析:(1)由反应“2Ag+(aq)+Cu(s)═Cu2+(aq)+2Ag(s)”可知,在反应中,Cu被氧化,失电子,应为原电池的负极,Ag+在正极上得电子被还原,电解质溶液为AgNO3。
(2)正极为活泼性比Cu弱的Ag,Ag+在正极上得电子被还原,电极反应为Ag++e=Ag,X电极为原电池的负极,Cu失去电子发生氧化还原反应:Cu-2e-=Cu2+。
(3)原电池中,电子从负极经外电路流向正极,本题中由Cu极经外电路流向Ag极。


科目:高中化学 来源: 题型:
【题目】在日本,金刚烷胺一直作为帕金森病的治疗药,并于1998年被批准用于流感病毒A型感染性疾病的治疗,金刚烷胺的合成路线如图所示。下列说法不正确的是

A. 金刚烷胶的分子式是C10H17N B. 金刚烷胺的一溴代物有四种
C. 该路线中的反应都属于取代反应 D. W的同分异构体中一定含有苯环
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】面对目前世界范围内的能源危机,甲醇作为一种较好的可再生能源,具有广泛的应用前景。
(1)已知在常温常压下反应的热化学方程式:
①CO(g)+2H2(g) ![]() CH3OH(g) ΔH1=-90 kJ·mol-1
CH3OH(g) ΔH1=-90 kJ·mol-1
②CO(g)+H2O(g) ![]() CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
CO2(g)+H2(g) ΔH2=-41 kJ·mol-1
写出由二氧化碳、氢气制备甲醇的热化学方程式:_______________________。
(2)在容积为V L的容器中充入a mol CO与2a mol H2,在催化剂作用下反应生成甲醇,平衡时的转化率与温度、压强的关系如图所示。

①p1________p2(填“大于”、“小于”或“等于”);
②在温度和容积不变的情况下,再增加a mol CO与2a mol H2,达到新平衡时,CO的转化率________(填“增大”、“减小”或“不变”,下同),平衡常数________。
(3)关于CO(g)+2H2(g) ![]() CH3OH(g) ΔH1=-90 kJ·mol-1 正确的是_____________________
CH3OH(g) ΔH1=-90 kJ·mol-1 正确的是_____________________
A.温度和压强一定时,混合气体的密度不再变化,证明已经达到平衡状态
B. 2V(CO)正= V(H2)逆
C.温度和体积一定时,容器内压强不变,证明已经达到平衡状态
D.百分比组成2W(CO)=W(H2),证明已经达到平衡状态
E.混合气体的平均相对分子质量不再改变的状态,证明已经达到平衡状态
F.温度越高越有利于该反应自发进行
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物F( )为一种高分子树脂,物质C的分子式为:C10H10Obr2;F的合成路线如下:
)为一种高分子树脂,物质C的分子式为:C10H10Obr2;F的合成路线如下:

已知:①A为苯甲醛的同系物,分子中无甲基,其相对分子质量为134;
②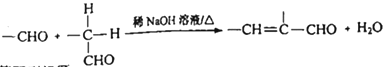
请回答下列问题:
(1)X的化学名称是_____________________________________。
(2)E生成F的反应类型为___________________________________。
(3)D的结构简式为________________________________。
(4)由B生成C的化学方程式为______________________________________。
(5)芳香族化合物Y是D的同系物,Y的同分异构体能与饱和Na2CO3溶液反应放出气体,分子中只有1个侧链,核磁共振氢谱显示有5种不同化学环境的氢,峰值面积比为6:2:2:1:1。写出两种符合要求的Y的结构简式____________、________________________。
(6)写出以甲醛、丙醛和乙二醇为主要原料合成软质隐形眼镜高分子材料-聚甲基丙烯酸羟乙酯( )的合成路线(无机试剂自选):__________________________。
)的合成路线(无机试剂自选):__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】材料是人类生存和发展的物质基础,合理使用材料可以改善人类生活。下列有关材料的说法中正确的是
A. 棉、麻、丝、毛及合成纤维完全燃烧都只生成C02和H20
B. 金属材料都是导体,非金属材料都是绝缘体
C. 天然橡胶通过硫化可增大强度和弹性
D. 玻璃是混合物,有固定的熔点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】把2.3 g钠投入38.8 g水中,发生化学反应。假设水蒸发损失1 g,所得溶液中溶质的质量分数为( )
A. 4.6% B. 7.7% C. 10.0% D. 8.0%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室可用少量的溴和足量的乙醇制备1,2-二溴乙烷。制备装置如下图:

下列说法中不正确的是( )
A. 使用恒压滴液漏斗的目的是防止有机物挥发,使漏斗内液体顺利滴下
B. 实验中为了防止有机物大量挥发,应缓慢升高反应温度到170℃
C. 装置C 中应加入氢氧化钠溶液,以吸收反应中可能生成的酸性气体
D. 实验过程中应用冷水冷却装置D,以避免溴的大量挥发
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL的酸式滴定管中,某浓度HCl溶液在30mL处,则该HCl溶液的体积为( )
A. 等于20mL B. 大于20mL C. 等于30mL D. 大于30mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com