
在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
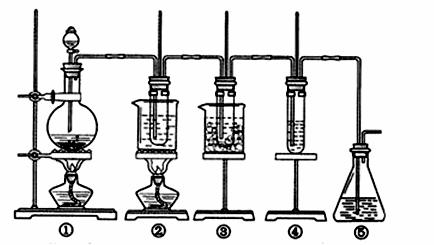
图中:①为氯气发生装置;②的试管里盛有15mL30%KOH 溶液.并置于水浴中; ③ 的试管里盛有15mL 8 % NaOH 溶液.并置于冰水浴中; ④ 的试管里加有紫色石蕊试液; ⑤ 为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加人一定量的二氧化锰.通过________________(填写仪器名称)向烧瓶中加人适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在① 与② 之间安装盛有___________(填写下列编号字母)的净化装置。
A.碱石灰 B.饱和食盐水 C.浓硫酸 D.饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:_______________________________
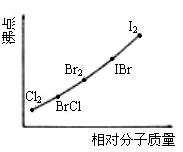
反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是________(填写编号字母);从②的试管中分离出该晶体的方法是________________(填写实验操作名称)
(3)本实验中制取次氯酸钠的离子方程式是:_______________________________
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为____色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | _______________________________________ |
| 然后溶液从无色逐渐变为____色 | _______________________________________________ |
【答案】
(1)分液漏斗 B
(2)碱溶液(或反应物)的浓度不同,反应温度不同 M 过滤
(3) Cl2 + 2OH-=ClO- + Cl一+H2O
(4)
| 红 | |
| 氯气与水反应生成的HClO将石蕊氧化为无色物质 | |
| 黄绿 | 继续通入的氯气溶于水使溶液呈黄绿色 |
【解析】本题为实验探究题,主要考查Cl2的制备,Cl2、Cl2-H2O及NaClO等物质的性质,并以此为依托考查考生观察、分析问题的能力。
(1)烧瓶中的MnO2与通过分液漏斗加入的浓盐酸发生反应,MnO2+4HCl(浓) 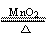 MnCl2+Cl2↑+2H2O,产生的Cl2中常因浓HCl易挥发而含有HCl,可通过盛有饱和食盐水的洗气瓶除去(浓H2SO4只能干燥Cl2,并不与HCl反应),碱石灰可同时吸收Cl2和HCl,而NaHCO3溶液则会引入新的杂质CO2)。
MnCl2+Cl2↑+2H2O,产生的Cl2中常因浓HCl易挥发而含有HCl,可通过盛有饱和食盐水的洗气瓶除去(浓H2SO4只能干燥Cl2,并不与HCl反应),碱石灰可同时吸收Cl2和HCl,而NaHCO3溶液则会引入新的杂质CO2)。
(2)比较装置②③中所给物质的特点及反应条件可知,制备KClO3和NaClO二者的条件差异在于反应物的浓度不同、反应温度不同;反应完毕后冷却②的试管有大量晶体析出,则该晶体的溶解度随温度升高而增大,故符合曲线M的特征,分离②中的固体与溶液可用过滤的方法。
(4)Cl2+H2O H++Cl-+HClO,生成的H+可使石蕊试液变红色,又由于HClO具有强氧化性,可把石蕊氧化为无色物质,故石蕊试液又变为无色,当然通入的Cl2过量时,水溶液中含较多Cl2而呈黄绿色。
H++Cl-+HClO,生成的H+可使石蕊试液变红色,又由于HClO具有强氧化性,可把石蕊氧化为无色物质,故石蕊试液又变为无色,当然通入的Cl2过量时,水溶液中含较多Cl2而呈黄绿色。


科目:高中化学 来源: 题型:
某钠盐溶液中可能含有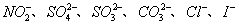 等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
等阴离子。某同学取5份此溶液样品,分别进行了如下实验:
①用pH计测得溶液pH大于7
②加入盐酸,产生有色刺激性气体
③加入硝酸酸化的AgNO3溶液产生白色沉淀,且放出有色刺激性气体
④加足量BaCl2溶液,产生白色沉淀,该沉淀溶于稀硝酸且放出气体,将气体通入品红溶液,溶液不褪色。
⑤加足量BaCl2溶液,产生白色沉淀,在滤液中加入酸化的(NH4)2Fe(SO4)溶液,再滴加KSCN溶液,显红色
该同学最终确定在上述六种离子中公含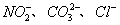 三种阴离子。
三种阴离子。
请分析,该同学只需要完成上述哪几个实验,即可得出此结论。
A. ①②④⑤ B. ③④ C. ③④⑤ D. ②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
明矾石是制取钾肥和氢氧化铝的重要原料,明矾石的组成和明矾相似,此外还含有氧化铝和少量氧化铁杂质。具体实验步骤如下图所示:

根据上述图示,完成下列填空:
(1)明矾石焙烧后用稀氨水浸出。配制500 mL稀氨水(每升含有39.20 g氨)需要取浓氨水(每升含有251.28 g氨)______________mL,用规格为___________mL量筒量取。
(2)氨水浸出后得到固液混合体系,过滤,滤液中除K+、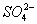 外,还有大量的
外,还有大量的 。检验
。检验 的方法是________________________________________________。
的方法是________________________________________________。
(3)写出沉淀物中所有物质的化学式_____________________________________。
(4)滤液Ⅰ的成分是水和______________。
(5)为测定混合肥料K2SO4、(NH4)2SO4中钾的含量,请完善下列步骤:
①称取钾氮肥试样并溶于水,加入足量__________溶液,产生白色沉淀。
②__________、__________、__________(依次填写实验操作名称)。
③冷却,称重。
(6)若试样为m g,沉淀的物质的量为n mol,则试样中K2SO4的物质的量为:__________mol(用含m、n的代数式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
以氯化钠和硫酸铵为原料制备氯化铵及副产品硫酸钠,工艺流程如下:

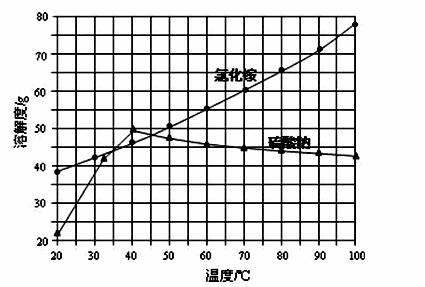
氯化铵和硫酸钠的溶解度随温度变化如下图所示。回答下列问题:
(1)欲制备10.7gNH4Cl,理论上需NaCl g。
(2)实验室进行蒸发浓缩用到的主要仪器有 、烧杯、玻璃棒、酒精灯等。
(3)“冷却结晶”过程中,析出NH4Cl晶体的合适温度为 。
(4)不用其它试剂,检查NH4Cl产品是否纯净的方法及操作是 。
(5)若NH4Cl产品中含有硫酸钠杂质,进一步提纯产品的方法是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
可用下图装置制取(必要时可加热)、净化、收集的气体是
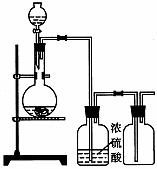
A 铜和稀硝酸制一氧化氮 B 氯化钠与浓硫酸制氯化氢
C 锌和稀硫酸制氢气 D 硫化亚铁与稀硫酸制硫化氢
查看答案和解析>>
科目:高中化学 来源: 题型:
下列除去杂质的方法正确的是
① 除去乙烷中少量的乙烯:光照条件下通入Cl2,气液分离;
② 除去乙酸乙酯中少量的乙酸:用饱和碳酸氢钠溶液洗涤,分液、干燥、蒸馏;
③ 除去CO2中少量的SO2:气体通过盛饱和碳酸钠溶液的洗气瓶;
④ 除去乙醇中少量的乙酸:加足量生石灰,蒸馏。
A.① ② B.② ④
C.③ ④ D.② ③
查看答案和解析>>
科目:高中化学 来源: 题型:
某研究小组进行与NH3有关的系列实验。
⑴从下图中挑选所需仪器,画出制取干燥NH3的装置简图(添加必要的塞子、玻璃导管、胶皮管。固定装置和尾气处理装置不用画),并标明所用试剂。

⑵将NH3通入溴水中,有N2生成,反应的化学方程式为 。
⑶为验证“同温同压下,相同体积的任何气体都含有相同数目的分子”,该小组同学设计了如图所示的装置,图中B管的容积是A管的2倍,活塞K1、K2、K3、K4、K5均(固定装置和尾气处理装置略;HCl和NH3均不溶于石蜡油,也不与之反应;装置气密性好)。
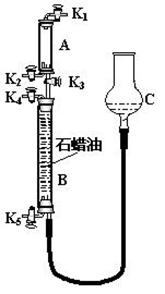
①在A管中充满与大气压强相等的干燥HCl气体。操作是 。
控制活塞K4、K5,调节C,使B管充满与A管同压的干燥NH3。
②缓缓开启K3,A管中的现象是 。要达到实验目的,当反应完成并恢复到室温时,B管中预期的现象是 ;若观察不到预期现象,主要原因是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述中正确的是 ( )
①标准状况下,1 L HCl和1 L H2O的物质的量相同;
②标准状况下,1 g H2和14 g N2的体积相同;
③28 g CO的体积为22.4 L;
④两种物质的物质的量相同,则它们在标准状况下的体积也相同;
⑤在同温同体积时,气体物质的物质的量越大,则压强越大;
⑥同温同压下,气体的密度与气体的相对分子质量成正比。
A.①②③ B.②⑤⑥
C.②③⑥ D.④⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)用50mL 0.50mol·L-1盐酸与50mL 0.55mol·L-1NaOH溶液在如下图所示的装置中进行中和反应。通过测定反应过程中放出的热量可计算中和热。回答下列问题:
①烧杯间填满碎泡沫塑料的作用是 。
|
(填“偏大”、“偏小”或“无影响”)
③若通过测定计算产生的热量为1.42kJ,请写该反应的
热化学方程式: 。
(2)①已知:CH4(g)+H2O(g)===CO(g)+3H2(g) ΔH=+206.2 kJ·mol-1
CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH=+247.4 kJ·mol-1
则以甲烷为原料制取氢气是工业上常用的制氢方法。CH4(g)与H2O(g)反应生成CO2(g)和H2(g)的热化学方程式为: 。
②由气态基态原子形成1 mol化学键释放的最低能量叫键能。已知表中所列键能数据, 则N2(g)+3H2(g)  2NH3(g) ΔH= kJ·mol-1。
2NH3(g) ΔH= kJ·mol-1。
| 化学键 | H—H | N—H | N≡N |
| 键能kJ·mol-1 | 436 | 391 | 945 |
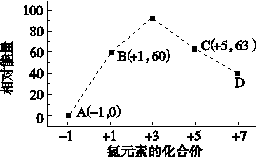
③一定条件下,在水溶液均为1 mol以下离子 Cl-、ClO-、ClO2-、ClO3-、ClO4-的能量(kJ)相对大小如下图所示,则3ClO-(aq)===ClO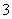 (aq)+2Cl-(aq)的ΔH= kJ·mol-1。
(aq)+2Cl-(aq)的ΔH= kJ·mol-1。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com