
| A.在SiO2晶体中,每个Si原子与4个O原子形成共价键 |
| B.在面心立方密堆积的金属晶体中,每个金属原子周围紧邻的有4个金属原子 |
| C.NaCl晶体中与每个Na+距离相等且最近的Cl—有6个; |
| D.CsCl晶体中与每个Cs+距离相等且最近的Cl—有8个 |
科目:高中化学 来源:不详 题型:填空题
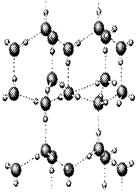
 用于估算化学反应的反应热(△H),化学反应的△H等于反应
用于估算化学反应的反应热(△H),化学反应的△H等于反应| 化学键 | F—D | F—F | B—B | F—B | C═D | D═D |
| 键能/kJ·mol-1 | 460 | 176 | 347.7 | 347 | 745 | 497.3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.②③⑤ | B.③⑤ | C.③④ | D.③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
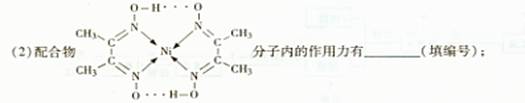
| A.氢键 | B.离子键 | C.共价键 | D.配位键 |
 等,其中碳原子采取sp2杂化的分子有 (填物质序号),预测HCHO
等,其中碳原子采取sp2杂化的分子有 (填物质序号),预测HCHO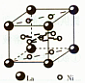
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
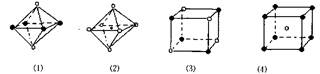
| A.(1)(3) | B.(2)(3) | C.(3)(4) | D.只有( 4) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.离子晶体中,一定存在离子键 | B.原子晶体中,只存在共价键 |
| C.金属晶体的熔、沸点均很高 | D.分子晶体中不一定含化学键 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.钠离子与氯离子之间通过静电吸引结合在一起 |
| B.与某个钠离子最接近的钠离子有12个 |
| C.某个钠离子周围的氯离子围成的空间结构为正八面体 |
| D.晶体中钠离子的半径比氯离子的半径小 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
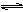 CH3CH2OH(g)+3H2O(g) △H=a kJ·mol-1
CH3CH2OH(g)+3H2O(g) △H=a kJ·mol-1
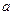 0(填“大于”或“小于”)。
0(填“大于”或“小于”)。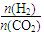 )比,平衡常数K值 (填“增大”、“减小”、或“不变”),对生成乙醇 (填“有利”或“不利”)。
)比,平衡常数K值 (填“增大”、“减小”、或“不变”),对生成乙醇 (填“有利”或“不利”)。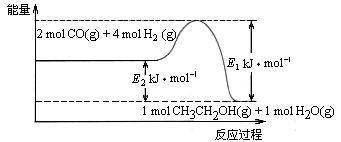
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.32 | B.65 | C.120 | D.150 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com