
【题目】医学上常用于杀菌消毒的物质是
A.工业酒精 B.75%乙醇溶液 C.生理盐水 D.10%葡萄糖水
科目:高中化学 来源: 题型:
【题目】我国古代就有湿法炼铜的记载“曾青得铁则化为铜”,反应为Fe+CuSO4=Cu+FeSO4。有关该反应的说法正确的是
A.Fe是氧化剂 B.CuSO4是还原剂
C.Fe被氧化 D.CuSO4发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各表述与示意图—致的是( )
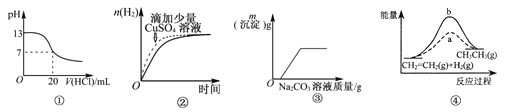
A.图①表示25℃时,用0.1 mol/L盐酸滴定20 mL 0.1 mol/L NaOH溶液, 溶液的pH随加入酸体积的变化
B.图②中表示常温下,两份少量等浓度的盐酸与过量锌粉反应时,其中一份滴加了少量硫酸铜溶液
C.图③表示10 mL 0.01 mol/LKMnO4酸性溶液与过量的0.1 mol/L H2C2O4溶液混合时(Mn2+是该反应的催化剂),n (Mn2+)随时间的变化
D.图④中a、b曲线分别表示反应CH2=CH2 (g) +H2(g) →CH3CH3 (g)△H < 0,使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烟气的脱硫(除SO2)技术和脱硝(除NOx)技术都是环境科学研究的热点。
(1)烟气脱硫、脱硝的环境意义是______________________;
(2)一种选择性催化脱硝(NO2)的原理为:6NO2+8NH3 ![]() 7N2+12H2O
7N2+12H2O
① 上述反应中被还原的元素是_________(填元素符号),反应中每转移3mol电子,生成标准状况下N2的体积为____________;
② 超音速飞机排放的尾气是平流层中NOx的主要来源.它们破坏臭氧层的主要机理为:
Ⅰ 、O3![]() O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
O+O2 Ⅱ 、NO+O3→NO2+O2 Ⅲ 、 NO2+O→ NO+O2
上述反应中NOx所起的作用是_____________;
(3)下表列出了2种燃煤烟气脱硫方法的原理。
方法Ⅰ | 用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4 |
方法Ⅱ | 用生物质热解气(主要成分CO、CH4、H2)将SO2在高温下还原成单质硫 |
①方法Ⅰ中用氨水吸收燃煤烟气中的SO2转化为NH4HSO3,是利用了SO2的___________性质(选填字母编号)。
A.漂白性 B.氧化性 C.还原性 D.酸性氧化物
②方法Ⅰ中氨水吸收燃煤烟气中SO2的化学反应为:2NH3+SO2+H2O=(NH4)2SO3
(NH4)2SO3+SO2+H2O=2NH4HSO3,能提高燃煤烟气中SO2去除率的措施有______(填字母).
A.增大氨水浓度 B.升高反应温度
C.使燃煤烟气与氨水充分接触 D.通入空气使HSO3-转化为SO42-
③采用方法Ⅰ脱硫,并不需要预先除去燃煤烟气中大量的CO2,原因是_________________(用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于N2(g)+3H2(g)![]() 2NH3(g) △H1KJ/mol,满足如下图像:
2NH3(g) △H1KJ/mol,满足如下图像:

(1)根据图判断△H1 0,T3 T4。(填“>”“<”“=”)
(2)若温度为T1且容器为2L的密闭容器下中,发生合成氨的反应,起始时通入2mol的N2和6mol的H2,10分钟达到平衡状态,此时NH3的体积分数为60%。则0到10min内用H2表示化学反应速率为_________mol/(L·min),N2的转化率为___________,反应开始和平衡状态体系的压强之比等于___________。
(3)若第(2)小问中反应体系达到平衡后,再通入1molN2和3mol的H2,则H2的转化率为___________(填“增大”“减小”或“不变”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,反应N2(g)+O2(g)2NO(g)在密闭容器中进行,下列措施不改变化学反应速率的是 ( )
A.恒容充入N2
B.缩小体积使压强增大
C.恒容充入氦气
D.恒压充入氦气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)两个试剂瓶各盛装质量相同的浓硫酸和浓硝酸,分别敞口放置一段时间后,两溶液质量关系为m(硫酸)_____ m(硝酸)(填“>”、“<”或“=”),由于浓硫酸和浓硝酸都具有强氧化性,所以冷的浓硫酸和浓硝酸都可以用_____(写金属名称)制容器盛放。
(2)制备CuSO4和Cu(NO3)2
①下列有四种制备Cu(NO3)2的途径,其中最佳途径是(选填字母)___
a. Cu![]() Cu(NO3)2
Cu(NO3)2
b. Cu![]() Cu(NO3)2
Cu(NO3)2
c. Cu![]() CuO
CuO ![]() Cu(NO3)2
Cu(NO3)2
d. Cu![]() CuSO4
CuSO4 ![]() Cu(NO3)2
Cu(NO3)2
② 向稀硫酸溶液中加入铜粉,然后通入热空气,可制得硫酸铜溶液,则发生反应的离子方程式为___________________________________。
(3)向200mL2mol/LHNO3溶液中加入足量铜粉,充分作用后,有m1g固体不溶物,继续 加入100mL 1mol/L硫酸溶液,充分作用后,还有m2g固体不溶物,则 m1 ________ m2(填“>”、“<”或“=”),两者质量相差g_____(若两者相等,则此问不答)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是一些常见的单质、化合物之间的转化关系图,有些反应中的部分物质和条件被略去。A、X、Y是常见金属单质,其中Y既能与强酸反应,又能与强碱反应;B、C、E是常见气体,G的焰色反应呈黄色;I的溶液呈黄色。

请回答下列问题:
(1)写出下列物质的化学式A__________、 F__________;
(2)说出黄绿色气体C的一种用途_________________________________;
(3)实验室检验H中所含的金属阳离子的方法是,先加____________________无明显现象,再加氯水,溶液变为_________色;
(4)写出Y和D溶液反应的离子方程式_________________________________________;
(5)写出C与H溶液反应的化学方程式__________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com