
下图所示为验证二氧化硫性质的微型实验,a、b、c、d是浸有相关溶液的棉球。试验时先将浓硫酸滴入装有亚硫酸钠固体的培养皿中。

则下列关于此实验现象,解释或结论以及对应关系均正确的是( )

B
【解析】
试题分析:在培养皿中浓硫酸与亚硫酸钠固发生反应产生SO2气体,中 a处发生反应:Br2+SO2+2H2O=H2SO4+2HBr。产物都是无色的,所以可以看到黄色变为无色,只是发生氧化还原反应,不能证明费金属性Br>S,产物;在b处SO2+H2O=H2SO3,H2SO3是酸,使紫色石蕊试液变为红色,正确;在c处可能是a处挥发的Br2单质氧化KI产生I2单质,也可能是SO2氧化KI产生I2单质而遇淀粉变为蓝色,因此不能证明具有SO2氧化性,错误;在d处SO2具有漂白性把品红溶液漂白为无色物质,前边a处产生的溴单质会把SO2氧化为硫酸而失去漂白性,因此d处红色褪为无色后随着SO2的减小红色又复原,由于没有加热,所以不能证明其漂白性不稳定,错误。
考点:考查二氧化硫性质的性质及相应的实验现象的知识。


科目:高中化学 来源:2015届辽宁省分校高三上学期期初考试化学试卷(解析版) 题型:选择题
氧化还原反应中,水的作用可以是氧化剂、还原剂、既是氧化剂又是还原剂、既非氧化剂又非还原剂等。下列反应与Br2+SO2+2H2O=H2SO4+2HBr相比较,水的作用不相同的是( )
A.2Na2O2+2H2O=4NaOH+O2↑ B.4Fe(OH)2+O2+2H2O=4Fe(OH)3
C.Cl2+H2O=HCl+HClO D.2Al+2NaOH+2H2O=2NaAlO2+3H2↑
查看答案和解析>>
科目:高中化学 来源:2015届辽宁沈阳市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
已知M2On2- 离子可与R2- 离子作用,R2- 被氧化为R单质,M2On2-的还原产物中,M为+3价;又如c(M2On2 )=0.3 mol?L 的溶液100 mL可与c(R2- )=0.6 mol?L 的溶液150 mL恰好完全反应,则n值为
A.4 B.5 C.6 D.7
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:填空题
(6分)根据下列信息回答问题。
(1)请用系统命名法对 ,命名:_____________;
,命名:_____________;
(2)HO(CH2)3COOH发生缩聚反应后所得缩聚物的结构结构简式:____________;
(3)一定条件下某烃M与H2按物质的量之比1:2加成生成C2H5C(CH3)3,则烃M的结构简式为_____________.
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:填空题
(9分)砷(As)广泛分布与自然界,砷与氮同主族,比氮多两个电子层。
(1)砷位于元素周期表中_____周期________族,其气态氢化物的稳定性比NH3_______(填“强”或“弱”);
(2)砷的常见酸性氧化物有As2O3和As2O5,请根据图中信息写出As2O3分解为As2O5的热化学方程式:________________________;

(3)已知:将酸滴入砷酸盐与KI混合的溶液中发生反应:AsO43-+2I―+2H+=AsO33-+I2+H2O.某研究性学习小组同学欲利用该反应原理,设计实验装置探究原电池原理,请你配合他们绘制原电池装置图,并回答下列问题:
若以石墨为电极,正极上发生的反应为______________.该电池工作时,当外电路中转移5mol电子时,则有_________molI2生成.
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
下列实验方案中,可达到预期目的的是( )
A.用萃取的方法分离Br2和CCl4混合物
B.加足量烧碱溶液过滤,出去混在镁粉中的少量铝粉
C.加入盐酸酸化的Ba(NO3)2溶液,可以鉴别Na2SO3和Na2SO4
D.用溶解、过滤的方法分离KNO3和NaCl的混合物
查看答案和解析>>
科目:高中化学 来源:2015届贵州省贵阳市高三年级8月摸底考试化学试卷(解析版) 题型:选择题
以“改革驱动,走向生态文明新世代”为主题的生态文明贵阳国际论坛2014年7月在贵阳召开,本次年会确定以植树造林增加碳汇的方式,实现“碳中和”目标。下列行为与此次目标不相符的是
A.采取“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”等方法,以提高空气质量
B.开发时能、风能、太阳能、地热能、核能等新能源,减少使用煤、石油等化石燃料
C.大力开采煤、石油和天然气,以满足经济发展的需要
D.大力发展新能源汽车,如混合动力汽车、电动汽车等,以减少碳、氮氧化物的排放
查看答案和解析>>
科目:高中化学 来源:2015届福建省高二上学期第二次月考化学试卷(解析版) 题型:选择题
在25℃时,密闭容器中X、Y、Z三种气体的浓度如下表: 下列说法错误的是( )
下列说法错误的是( )
物质 | X | Y | Z |
初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
 A.反应达到平衡时,X的转化率为50%
A.反应达到平衡时,X的转化率为50%
 B.改变温度可以改变此反应的平衡常数
B.改变温度可以改变此反应的平衡常数
 C.反应可表示为X+3Y
C.反应可表示为X+3Y 2Z,平衡常数为1600
2Z,平衡常数为1600
 D.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.增大压强使平衡向生成Z的方向移动,平衡常数增大
查看答案和解析>>
科目:高中化学 来源:2015届福建省高三上学期第二次质量检查化学试卷(解析版) 题型:实验题
(15分)I2O5是白色固体,遇水生成碘酸(HIO3)。I2O5可用于检验并定量测定空气中的CO,在常温下发生的反应为 5CO+I2O5=5CO2+I2 (空气中其余气体不与I2O5反应)。
实验一:制取I2O5
将碘酸加热至90~110 ?C使其部分脱水,再升温至220~240 ℃并恒温4 h,使反应完全。接着慢慢冷却至室温,密封保存,即得五氧化二碘。
(1)写出碘酸制I2O5的化学方程式: 。
(2)在制得的I2O5固体中含有少量I2杂质,提纯的方法是 (填标号);
A.过滤 B.蒸发结晶 C.蒸馏 D.升华
用提纯方法用到的玻璃仪器为 (填标号)。
A.圆底烧瓶 B.烧杯 C.普通漏斗 D.酒精灯 E.玻璃棒
实验二:检验空气中CO
利用下图装置检验空气中是否存在CO。
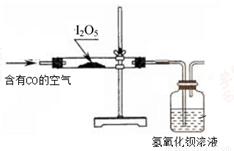
(3)能说明空气中含有CO的现象是 。
(4)倘若要从广口瓶中出现浑浊来判断空气中含有CO,请写出改进的实验方案: 。
实验三:测定空气中CO的含量
(5)将I2O5与CO反应生成的碘单质用硫代硫酸钠滴定(反应为I2+2Na2S2O3=Na2S4O6+2NaI),即可根据消耗硫代硫酸钠的量来计算空气中CO的含量。若某次实验时测得参与反应的空气体积为a mL(标准状况下),滴定过程中,共消耗v mL c mol·L-1 Na2S2O3溶液。则该空气样品中CO的体积分数是 。
(6)该实验测定出来的结果不可信,最大可能的原因是: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com