
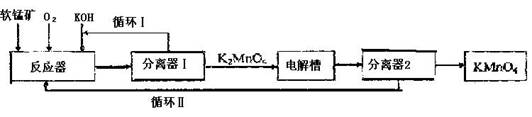
KMnO4是一种常用的强氧化剂,工业上可以以软锰矿(主要成分MnO2)为原料,通过液相法生产。即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4,再用镍板作阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:
![]()
![]() 回答下列问题:
回答下列问题:
![]() (1)写出反应器中反应的方程式
(1)写出反应器中反应的方程式
![]() (2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿中Al、 Si的氧化物含量较高,会导致KOH消耗量偏高,用方程式表示KOH消耗偏高的原因 、 。
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿中Al、 Si的氧化物含量较高,会导致KOH消耗量偏高,用方程式表示KOH消耗偏高的原因 、 。
![]() (3)写出电解槽中阴极和阳极的电极反应方程式
(3)写出电解槽中阴极和阳极的电极反应方程式
阴极: ;阳极: 。
在电解法中循环Ⅰ、Ⅱ中利用的共同物质是 。
![]() (4)在传统工艺中,得到K2MnO4后,向其中通入CO2制备KMnO4,配平方程式
(4)在传统工艺中,得到K2MnO4后,向其中通入CO2制备KMnO4,配平方程式
![]() K2MnO4+ CO2= KMnO4+ MnO2+ K2CO3
K2MnO4+ CO2= KMnO4+ MnO2+ K2CO3
![]() 根据上述反应,从Mn元素的角度考虑KMnO4的产率最高为 。与该传统工 艺相比,电解法的优势是 、 。
根据上述反应,从Mn元素的角度考虑KMnO4的产率最高为 。与该传统工 艺相比,电解法的优势是 、 。
 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
【化学——选修2:化学与技术】(15分)
KMnO4是一种常用的强氧化剂,工业上以软锰矿(主要成分MnO2)为原料,通过液相法生产。即在反应器中碱性条件下用氧气氧化KnO2得到K2MnO4,分离后得到K2MnO4,再在电解槽中用铂板作用阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:
回答下列问题:
(1)写出反应器中反应的方程式_______
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量较低的贫矿中Al的氧化物含量较高,会导致KOH消耗量偏离,用离子方程式表示KOH消耗偏高的原因____。
(3)写出电解槽中阴极和阳极的电极反应方程式阴极:_______ :阳极:____。
(4)在传统工艺中,得到K2MnO4后,向其溶液中避入CO2制备KMnO4,配平方程式:
K2MnO4+_______CO2=_______KMnO4+_______ MnO2+ _______K2CO3
将所得到的KMnO4配成0.1mol·L-1KMnO4溶液,滴定20.00 rnL未知浓度的FeCl2液,消耗KMnO4溶液30.00 mL。滴定达到终点时的现象为:_______ ,则FeCl2溶液的浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源: 题型:
(12分).KMnO4是一种常用的强氧化剂,工业上可以以软锰矿(主要成分MnO2)为原料,通过
液相法生产。即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4,再
用镍板作阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:
回答下列问题:
(1)写出反应器中反应的方程式
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿中Al、
Si的氧化物含量较高,会导致KOH消耗量偏高,用方程式表示KOH消耗偏高的原因
、 。
(3)写出电解槽中阴极和阳极的电极反应方程式
阴极: ;阳极: 。
在电解法中循环Ⅰ、Ⅱ中利用的共同物质是 。
(4)在传统工艺中,得到K2MnO4后,向其中通入CO2制备KMnO4,配平方程式
K2MnO4+ CO2= KMnO4+ MnO2+ K2CO3
根据上述反应,从Mn元素的角度考虑KMnO4的产率最高为 。与该传统工
艺相比,电解法的优势是 、 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年河北省唐山市高三上学期摸底考试理科综合化学试卷 题型:填空题
【化学——选修2:化学与技术】(15分)
KMnO4是一种常用的强氧化剂,工业上以软锰矿(主要成分MnO2)为原料,通过液相法生产。即在反应器中碱性条件下用氧气氧化KnO2得到K2MnO4,分离后得到K2MnO4,再在电解槽中用铂板作用阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:

回答下列问题:
(1)写出反应器中反应的方程式_______
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量较低的贫矿中Al的氧化物含量较高,会导致KOH消耗量偏离,用离子方程式表示KOH消耗偏高的原因____。
(3)写出电解槽中阴极和阳极的电极反应方程式阴极:_______ :阳极:____。
(4)在传统工艺中,得到K2MnO4后,向其溶液中避入CO2制备KMnO4,配平方程式:
K2MnO4+_______CO2= _______KMnO4+_______ MnO2+ _______K2CO3
将所得到的KMnO4配成0.1mol·L-1KMnO4溶液,滴定20.00 rnL未知浓度的FeCl2液,消耗KMnO4溶液30.00 mL。滴定达到终点时的现象为:_______ ,则FeCl2溶液的浓度为_______mol/L。
查看答案和解析>>
科目:高中化学 来源:09-10年建湖二中高二下学期期末考试化学卷 题型:填空题
(12分).KMnO4是一种常用的强氧化剂,工业上可以以软锰矿(主要成分MnO2)为原料,通过
液相法生产。即在碱性条件下用氧气氧化MnO2得到K2MnO4,分离后得到K2MnO4,再
用镍板作阳极,铁作阴极电解K2MnO4溶液得到KMnO4,简略生产过程如下所示:

回答下列问题:
(1)写出反应器中反应的方程式
(2)生产过程中最好使用含MnO280%以上的富矿,因为MnO2含量最低的贫矿中Al、
Si的氧化物含量较高,会导致KOH消耗量偏高,用方程式表示KOH消耗偏高的原因
、 。
(3)写出电解槽中阴极和阳极的电极反应方程式
阴极: ;阳极: 。
在电解法中循环Ⅰ、Ⅱ中利用的共同物质是 。
(4)在传统工艺中,得到K2MnO4后,向其中通入CO2制备KMnO4,配平方程式
K2MnO4+ CO2= KMnO4+ MnO2+ K2CO3
根据上述反应,从Mn元素的角度考虑KMnO4的产率最高为 。与该传统工
艺相比,电解法的优势是 、 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com