
科目:高中化学 来源: 题型:
肼(N2H4)是火箭发动机的一种燃料,反应时N2O4为氧化剂,生成N2和水蒸气。已知:
N2(g)+2O2(g)=N2O4(g) ΔH=+8.7 kJ·mol-1
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH=-534.0 kJ·mol-1
下列表示肼跟N2O4反应的热化学方程式,正确的是
A. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ΔH=-542.7 kJ·mol-1
B. 2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ΔH=-1059.3 kJ·mol-1
C. N2H4(g)+ 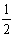 N2O4(g)=
N2O4(g)= N2(g)+2H2O(g) ΔH=-1076.7 kJ·mol-1
N2(g)+2H2O(g) ΔH=-1076.7 kJ·mol-1
D.2N2H4(g)+N2O4(g)=3N2(g)+4H2O(g) ΔH=-1076.7 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应C(s)+2NO(g) ====N2(g)+CO2(g)+Q kJ·mol-1。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
| 时间(Min) 浓度(mol·L-1) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①T1℃时,该反应的平衡常数K= ;
②30min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是 (填字母编号)。
a.加入一定量的活性炭 b.通人一定量的NO
c.适当缩小容器的体积 d.加入合适的催化剂
③若30min后升高温度至T2℃,达到平衡时,容器中NO、N2、CO2的浓度之比为5:3:3,则Q 0(填 “>”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子一定能在指定环境中大量共存的是
A.在c(H+)=10-10 mol/L的溶液中: Al3+ 、NH 、Cl- 、NO
、Cl- 、NO
B.pH值为1的溶液: Fe3+、Na+ 、SO42-、HCO3—
C.水电离出来的c(H+)=10-12mol/L的溶液: K+、NH4+、Cl-、ClO-
D.pH值为13的溶液: K+ 、SO 、Na+、AlO2—
、Na+、AlO2—
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)今有2H2+O2 2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
2H2O反应,构成燃料电池,则电极反应式为:负极____________________、正极__________________。
(2)如把H2改为甲烷,KOH做导电物质,则负极电极反应式为_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
氰气的化学式为(CN)2,结构式为N≡C—C≡N,性质与卤素相似,下列叙述正确的是
A.在一定条件下可发生加成反应
B.分子中N≡C键的键长大于C—C键的键长
C.分子中含有2个σ键和4个π键
D.不和氢氧化钠溶液发生反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列事实不能用勒夏特列原理解释的是
A. FeS不溶于水,但能溶于稀盐酸中 B.钢铁在潮湿的空气中容易生锈
C.实验室中常用排饱和食盐水的方式收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
查看答案和解析>>
科目:高中化学 来源: 题型:
合成尿素的反应是分作两步进行的:
① 2CO2(g)+ NH3(g) H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
H2NCOONH4(aq)(氨基甲酸铵) △H =-159.47kJ/mol
②H2NCOONH4(aq) CO(NH2)2(aq)+ H2O(l) △H =-28.49kJ/mol
CO(NH2)2(aq)+ H2O(l) △H =-28.49kJ/mol
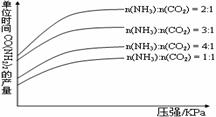
在生产条件下,单位时间内获得尿素的产量与压强和n(NH3):n(CO2)的关系如右图所示。生产过程中n(NH3):n(CO2)的最佳配比为 ,而实际实际生产条件下,往往使n(NH3):n(CO2)≥3,这是因为 。在得到的尿素溶液中会含有少量的氨基甲酸铵,除去这种杂质最简便的方法是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com