
【题目】甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,记录如下
表,其中记录合理的是
甲 | K2SO4、BaCl2、NH4NO3 |
乙 | NaCl、Ca(OH)2、K2CO3 |
丙 | HCl、Na2SO3、NaCl |
丁 | K2SO4、NaNO3、KCl |
A.甲 B.乙 C.丙 D.丁
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】(1) 物质的量浓度相同的醋酸和氢氧化钠溶液混合后,溶液中CH3COO-和Na+浓度相等,则醋酸体积__________氢氧化钠溶液体积 (填“>”“=”“<”)。
(2)pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后溶液,溶液中c(Na+)___________c(CH3COO-)(填“>”“=”“<”)。
(3)某温度(t℃)时,水的KW=10-13,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,若所得混合液为中性,则a∶b___________;若所得混合液的pH=2,则a∶b___________。
(4)室温下,若某pH值的硫酸溶液中水电离的c(H+)=1.0×10-amol·L-1,而相同pH值的硫酸铝溶液中水电离出的c(H+)=1.0×10-b mol·L-1,(已知a.b均小于14的正整数),那么a和b之间满足的数量关系是____________(用一个等式和一个不等式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值,下列说法正确的是
A. 反应KClO3+6HCl=3Cl2+KCl+3H2O,每生成1.5molCl2转移电子数为2.5NA
B. 标准状况下,11.2LNO与11.2LO2混合后所含分子数为0.75NA
C. 1L 0.1 molL-1NH4Cl溶液中NH4+的数目为0.1NA
D. 40gSiC中含有Si—C键的数目为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1)写出该反应的平衡常数表达式:K= 。已知:K300℃>K350℃,则该反应是 热反应。
(2)用O2表示从0~2 s内该反应的平均速率v= 。
(3)能使该反应的反应速率增大,且平衡向正反应方向移动的是 。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列五种物质中,用序号填写①Ar ②![]() ③H2SO4④
③H2SO4④![]() ⑤NaOH
⑤NaOH
只存在共价键的是________________,只存在离子键的是_______________________,
既存在离子键又存在共价键的是________________,不存在化学键的是____________。
属于共价化合物的是_______________,属于离子化合物的是__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为向一定量AlCl3溶液中加入NaOH溶液后,产生Al(OH)3白色沉淀的质量与OH-的物质的量之间的关系曲线。请回答下列问题:
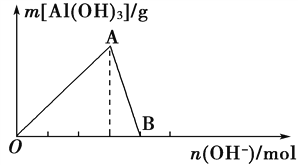
(1)A点时已参加反应的AlCl3和NaOH的物质的量之比为_______________________。
(2)OB段曲线所表示的反应,用一个离子方程式表示为____________________。
(3)向B处生成的溶液中通入过量二氧化碳,可观察到的现象是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数为NA,则下列说法正确的是
A.15g甲基(-CH3)所含有的电子数是9NA
B.7.8g ![]() 中含有的碳碳双键数为0.3NA
中含有的碳碳双键数为0.3NA
C.1mol C2H5OH和1mol CH3CO18OH反应生成水的中子数为8NA
D.标准状况下,11.2L己烷所含分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】质量分数为a%,物质的量浓度为c mol/L的KOH溶液,蒸发溶剂,恢复到原温度,若质量分数变为2a%,则物质的量浓度变为
A. 大于2c mol/L B. 等于 2c mol/L C. 小于2c mol/L D. 在 c mol/L~2c mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com