
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:阅读理解
查看答案和解析>>
科目:高中化学 来源:浙江省东阳中学2009-2010学年高二下学期期中考试化学试题 题型:022
一定温度下,将3 mol A气体和1 mol B气体通人一密闭容器中,发生如下反应:3A(g)+B(g)![]() nC(g).请填写下列空白:
nC(g).请填写下列空白:
(1)
若容器体积固定为2 L,2 min时测得剩余0.6 mol B,C的浓度为0.4 mol·L-1.①2 min内,A的平均反应速率为________;n=________;
②若反应从起始经4 min达到平衡,平衡时C的浓度________0.8 mol/L(填“>”、“<”或“=”);假设此时C的体积分数为x%
③若改变起始物质加入的量,欲使反应达到平衡时C的体积分数仍为x%,则起始加入的A、B、C三种物质的物质的量a、b、c之间应该满足的关系式为________、________.(分别用含a、c和含b、c的两个式子表示)
(2)
若维持容器压强不变:其它条件均与题(1)相同①此时达到平衡时C的体积分数为y%,则比较x________y(填“>”、“<”、“=”);
②改变起始物质加入的量,欲使反应达到平衡时C的体积分数仍为y%,则起始加入的A、B、C三种物质的物质的量a、b、c之间应该满足的关系式为________.
查看答案和解析>>
科目:高中化学 来源:2008-2009学年度山东省莱阳一中高三第一学期学段检测、化学试卷 题型:013
|
将下列物质加入或通人紫色石蕊溶液中,不能使其褪色的是 | |
| [ ] | |
A. |
SO2 |
B. |
Cl2 |
C. |
Na2O2 |
D. |
NaClO |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年湖北省荆州市高三毕业班质量检查(Ⅰ)化学试卷(解析版) 题型:实验题
实验室用铜制取硫酸铜,将适量硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全,通过蒸发、结晶得到硫酸铜晶体。
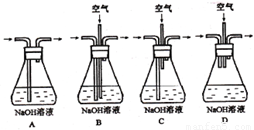
(1)为了节约原料,硫酸和硝酸的物质的量之比最佳为:_ ;为了吸收该反应中产生的尾气,应选择下列装置(填字母)。
(2)为符合绿色化学的要求,某研究性学习小组设计了如下两种方案:
方案1:以空气为氧化剂。将铜粉在仪器B中反复灼烧,使铜与空气充分反应生成氧化铜,再将氧化铜与稀硫酸反应。
方案2:将空气或氧气直接通人到铜粉与稀硫酸的混合物中,发现在常温下几乎不反应。向反应液中加少量FeSO4,即发生反应,生成硫酸铜。反应完全后,加物质甲调节pH,铁元素全部沉淀(一般认为铁离子的浓度下降到10-5mol·L-1,就认为沉淀完全),然后过滤、浓缩、结晶。
已知:Ksp(Cu(OH)2]=10-22, Ksp[Fe(OH)2]=10-16,Ksp[Fe(OH)3]=10-38
请回答下列问题:
①方案1中的B仪器名称是_。
②为了使铁元素全部沉淀,应调节pH至少为_。
③方案2中甲物质可选用的是_。
A. CaO B. NaOH C. CuCO3 D. Cu2(OH)2CO3 E. Fe2(SO4)3
④反应中加人少量FeSO4可加速铜的氧化,用离子方程式解释其原因 、
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com