
【题目】下列关于氯气的叙述正确的是
A.铁丝在氯气中燃烧生成FeCl2
B.红热的铜丝在氯气中剧烈燃烧,产生棕黄色的烟
C.氯气、液氯和氯水都是纯净物,都有漂白性
D.用氯气对生活用水进行消毒的原因是氯气本身能杀灭细菌
 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】短周期主族元素a、b、c、d、e的原子序数依次增大,b是地壳中含量最高的元素,e的单质的熔点在同周期元素中最高,a、b的原子序数之和等于e的原子序数,d原子的核外电子层数等于最外层电子数:分别向cdb2溶液、c2eb3溶液中通入气体ab2,产生沉淀的质量与通入气体的体积的定性关系都可用右图表示。下列说法不正确的是
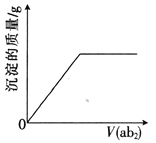
A. 原子半径:c>d>e>a>b
B. 工业上通常采用ab高温还原d2b3的方法冶炼d的单质
C. 同温下,0.1mol·L-1c2eb3溶液的pH大于0.1mol·L-1c2ab3溶液
D. 简单氢化物的热稳定性:b>a>e
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关物质的转化关系如图所示(部分物质与条件己略去).A是最常见的无色液体,B、C是常见的金属单质,D、E是气体单质,且D在空气中的含量最多,F 是一种具有磁性的化合物,H是既能与强酸反应又能与强碱反应的氧化物:I具有耐高温、抗冲击、导热性好的优良性质,广泛应用于电子工业、陶瓷工业中. 
请回答下列问题:
(1)H的化学式为 .
(2)D 的电子式为 .
(3)K出反应①的化学方程式: .
(4)写出G的水溶液与C的硝酸盐溶液反应的方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应原理中,不符合工业冶炼金属实际情况的是
A.2HgO![]() 2Hg+O2↑ B.4Al+3MnO2
2Hg+O2↑ B.4Al+3MnO2![]() 2Al2O3+3Mn
2Al2O3+3Mn
C.2MgO![]() 2Mg+O2↑ D.4CO+Fe3O4
2Mg+O2↑ D.4CO+Fe3O4![]() 3Fe+4CO2
3Fe+4CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】生理盐水是指质量分数为0.9%的NaCl溶液.下列有关该溶液说法正确的是( )
A.100g溶液中含有0.9 g NaCl
B.100 g水中含有0.9 g NaCl
C.100 g溶液中含有0.9 mol NaCl
D.100 g水中含有0.9 mol NaCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某探究小组设计如右图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。查阅资料,有关信息如下:
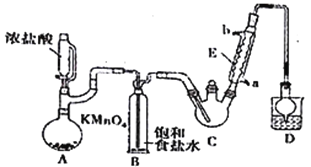
①制备反应原理:C2H5OH+4Cl2→CCl3CHO+5HCl
可能发生的副反应: C2H5OH+HCl→C2H5Cl+H2O;
CCl3CHO+HClO→CCl3COOH(三氯乙酸)+HCl
②相关物质的部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
相对分子质量 | 46 | 147.5 | 163.5 | 64.5 |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇 三氯乙醛 | 微溶于水,可溶于乙醇 |
(1)仪器A中发生反应的化学方程式为_________________________________。
(2)装置B的作用是_________________。该实验在装置中有一处缺陷,即缺少氯气的干燥裝置,缺少该装置可能导致装置C 中副产物______________(填化学式)的量增加;冷凝管的进水口是________(填“a”或“b”);
(3)装置中球形冷凝管的作用是______________________,写出D中所有可能发生的无机反应的离子方程式___________________________________。
(4)反应结束后,从C中的混合物中分离出CCl3COOH的方法是_________________________。
(5)测定产品纯度:称取产品0.50g配成待测溶液,加0.1000 molL-1碘标准溶液20.00 mL,再加入适量Na2CO3溶液,反应完全后,加盐酸调节溶液的pH,立即用0.02000 molL-1Na2S2O3溶液滴定至终点。进行三次平行实验,测得消耗Na2S2O3溶液20.00mL。则产品的纯度为_____________;(计算结果保留两位有效数字)滴定的反应原理:CCl3CHO+OH-==CHCl3span>+HCOO- HCOO-+I2== H++2I-+CO2↑ I2+2S2O32-==2I-+ S4O62-
(6)为证明三氯乙酸的酸性比乙酸强。某学习小组的同学设计了以下三种方案,你认为能够达到实验目的的是___________。
a.分别测定0.1mol·L-1两种酸溶液的pH,三氯乙酸的pH 较小
b.用仪器测量浓度均为0.1mol·L-1 的三氯乙酸和乙酸溶液的导电性,测得乙酸溶液的导电性弱
c.测定等物质的量浓度的两种酸的钠盐溶液的pH,乙酸钠溶液的pH 较大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2015年巴黎气候变化大会规定:本世纪实现温室气体净零排放.下列物质燃烧时能实现二氧化碳零排放的是( )
A.天然气
B.氢气
C.水煤气
D.煤炭
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在炼锌厂和炼钢厂废弃的含锌烟道灰中,含有30%~50%的氧化锌,另含少量Fe2O3、CuO、SiO2、MnO等物质,可用该烟道灰为原料生产草酸锌晶体(ZnC2O4·2H2O)。
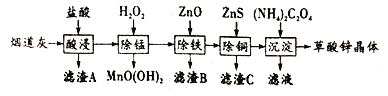
请回答下列问题:
(1)为了提高漫出速率,除将烟道灰处理得更细外,还可采取的措施有______ (写出一条)。
(2)证明除铁工序中Fe3+已经沉淀完全的实验步骤及现象是__________.
(3)上述流程中除铁与除铜的顺序不能颠倒,否则除铁率会减小,其原因是__________.
(4)己知: 常温下,Ksp[Fe(OH)3]=8.0×10-38.当加入ZnO控制反应液pH=5.0时,溶液中c(Fe3+)=_________.
(5)草酸能使酸性高锰酸钾溶液褪色,试写出相关反应的离子方程式:___________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在生物体内含量很少,但必不可少的微量元素有( )
A. Fe Mn Zn Mg
B. Zn Cu Mn Ca
C. H O Na Mg
D. Zn Cu B
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com