
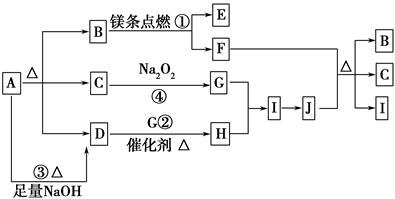
 2MgO+C,请填写以下空白:
2MgO+C,请填写以下空白:科目:高中化学 来源:不详 题型:单选题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.由题目信息知:KMnO4的氧化性比MnO2的强 |
| B.制备氯气的整个实验过程中,只需要使用氧化剂与还原剂 |
| C.用排气法收集不需要利用其他试剂就能确定集气瓶中已收集满气体 |
| D.用足量MnO2与含有4 mol HCl的浓盐酸在加热条件下反应,得到Cl2的物质的量小于1 mol |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.液溴易挥发,在存放液溴的试剂瓶中应加水封 |
| B.能使湿润的淀粉KI试纸变蓝色的物质一定是Cl2 |
| C.某溶液中加入CCl4,CCl4层显紫色,证明原溶液中存在I- |
| D.某溶液中加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硅燃烧产物对环境产生的污染,容易得到有效控制 |
B.从Si(s)+O2(g)  SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多 SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多 |
| C.自然界中硅的贮存量丰富,可以从自然界直接获得单质硅 |
| D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
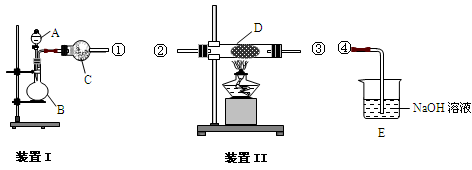
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
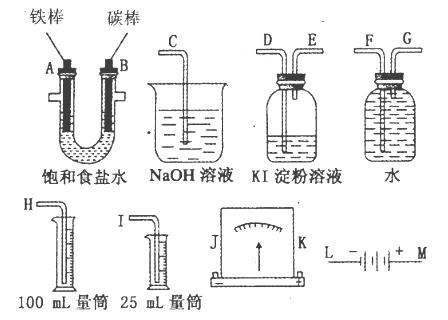
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
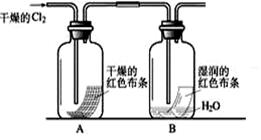

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com