
在热的稀硫酸中溶解了11.4 g FeSO4固体,当加入50 mL 0.5 mol·L-1 KNO3溶液时,其中的Fe2+全部转化成Fe3+,KNO3也完全反应并放出NxOy气体。
(1)推算出x=________;y=________。
(2)配平该反应的方程式:
FeSO4+____KNO3+____H2SO4===____K2SO4+____Fe2(SO4)3+____ (NxOy)+____H2O(配平时x、y用具体数值表示,物质填在
(NxOy)+____H2O(配平时x、y用具体数值表示,物质填在 中)。 (3)反应中氧化产物是________。
中)。 (3)反应中氧化产物是________。
(4)用双线桥法表示该反应中的电子转移方向和数目:___________________ ______________________________________ ___________________________。
___________________________。
科目:高中化学 来源: 题型:
已知苯甲醛与乙酸酐[(CH3CO)2O]在一定条件下可以通过Perkin反应生成肉桂酸,反应方程式(已配平)如下:
苯甲醛 肉桂酸
(1)1mol苯甲醛与足量银氨溶液在水浴条件下反应最多能生成_____ _mol银单质;写出肉桂酸完全加氢后产物的分子式 。
(2)上述反应中的产物M能与碳酸氢钠反应并放出气体,则M的结构简式是 。
(3)溴苯(C6H5Br)与丙烯酸乙酯(CH2=CHCOOC2H5)在氯化钯催化下可直接合成肉桂酸乙酯,该反应属于Beck反应,其反应方程式为
(不要求标出反应条件),该反应类型属于_______________。
 |
(4)已知具有五元环和六元环结构的缩醛比较稳定。写出用乙二醇(HOCH2CH2OH)保护苯甲醛中醛基生成的缩醛B(分子式:C9H10O2)的结构简式_________________。
(5)缩醛B(分子式:C9H10O2)符合以下条件的同分异构体有两种,写出它们的结构简式_________ ____。
①苯环上只有一个取代基;②能发生水解反应和银镜反应。
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L密闭容器中,保持恒温,加热KClO3和MnO2固体混合物制取O2,5min后,生成
O232克,则此反应的平均速率可表示为( )
A . v(O2)=3.2g·L-1·min-1 B. v(O2)=0.1 mol·L-1·min-1
C. v(KCl)=0.1 mol·L-1·min-1 D. v(KClO3)=0.0667 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
把6 molA气体和5 molB气体混合放入4L恒容密闭容器中。在一定条件下发生反应:3A(g)+B(g)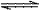 2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC。又知在此时D的平均速率为O.15 mol·L-1·min-1。
2C(g)+xD(g),经过5 min后达到化学平衡,此时生成2 molC。又知在此时D的平均速率为O.15 mol·L-1·min-1。
求:(1)平衡时A的物质的量浓度;
(2) B的转化率;
(3) x的值。(要求写出计算过程)
查看答案和解析>>
科目:高中化学 来源: 题型:
将SO2通入足量Fe2(SO4)3溶液中,完全反应后再加入K2CrO4溶液,发生的两个化学反应为SO2+2Fe3++2H2O===SO42-+2Fe2++W ①,Cr2O72-+aFe2++bH+―→Cr3++Fe3++H2O ②。下列有关说法正确的是 ( )。
A.还原性:Cr3+>SO2
B.方程式②中,a=6,b=7
C.Cr2O72-能将Na2SO3氧化成Na2SO4
D.方程式①中W为OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是 ( )。
A.石油裂解、煤的气化、海水制镁等过程中都包含化学变化
B.可通过电解熔融MgCl2来制取金属镁,故也能通过电解熔融AlCl3来制取
铝
C.铝热剂、盐酸、水玻璃、双氧水、明矾均为混合物
D.Na2O2、MgCl2、NaOH、NH4Cl均为含共价键的离子化 合物
合物
查看答案和解析>>
科目:高中化学 来源: 题型:
取少量Fe2O3粉末(红棕色)加入适量盐酸,发生反应的化学方程式:___________________________________________________,
反应后得到的溶液呈________色。用此溶液分别做如下实验:
(1)取少量溶液置于试管中,滴入几滴NaOH溶液,可观察到有红褐色沉淀生成,反应的化学方程式为_____________________________________________
________________________________________________________________,此反应属于________(填反应类型)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈________色,即制得Fe(OH)3胶体。
(3)取另一只小烧杯也加入20 mL蒸馏水,向烧杯中加入1 mL FeCl3溶液,振荡均匀后,将此烧杯(编号甲)与盛有Fe(OH)3胶体的烧杯(编号乙)一起放置于暗处,分别用激光笔照射烧杯中的液体,可以看到________烧杯中的液体产生丁达尔效应。这个实验可以用来区别_______________________________。
(4)用Fe(OH)3胶体进行下列实验:
①将其装入U形管中,用石墨电极接通直流电,通电一段时间后,发现阴极附近的颜色加深,这说明____________________________________________
_________________________________________________________________,这种现象称为________。
②向其中加入饱和(NH4)2SO4溶液发生的现象是________________,原因是________________ _____________________________________________
_____________________________________________ ______________________________________________________________________,
______________________________________________________________________,
③向其中滴入过量稀硫酸,现象是________________,其原因是___________ _________________________________________________________________。
④提纯此分散系常用的方法是______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在乙酸、乙醇、乙酸乙酯、水构成的平衡体系中,加入少量含18O的水:H218O,一段时间后,可以检测到18O在哪些物质中
A.乙酸、乙酸乙酯、水 B.乙醇、乙酸乙酯、水
C.乙醇、水 D.乙酸、水
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com