


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 (2008?广东)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定滴定反应的终点.如图所示是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线.下列示意图中,能正确表示用NH3?H2O滴定HCl和CH3COOH混合溶液的滴定曲线的是( )
(2008?广东)电导率是衡量电解质溶液导电能力大小的物理量,根据溶液电导率的变化可以确定滴定反应的终点.如图所示是KOH溶液分别滴定HCl溶液和CH3COOH溶液的滴定曲线.下列示意图中,能正确表示用NH3?H2O滴定HCl和CH3COOH混合溶液的滴定曲线的是( )查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
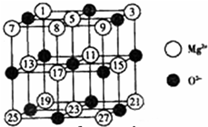 (2008?广东)镁、铜等金属离子是人体内多种酶的辅因子.工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁.
(2008?广东)镁、铜等金属离子是人体内多种酶的辅因子.工业上从海水中提取镁时,先制备无水氯化镁,然后将其熔融电解,得到金属镁.| 氧化物 | NaF | MgF2 | SiF4 |
| 熔点/K | 1266 | 1534 | 183 |
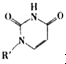 或Cu(I)(I表示化合价为+1)时,分别形成a和b:
或Cu(I)(I表示化合价为+1)时,分别形成a和b: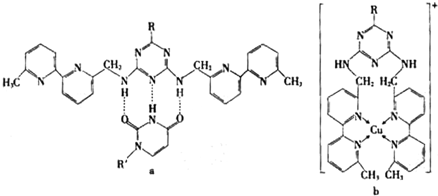
查看答案和解析>>
科目:高中化学 来源: 题型:013
(2008,广东,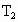 )海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是
)海水是一个巨大的化学资源宝库,下列有关海水综合利用的说法正确的是
[ ]
A.海水中含有钾元素,只需经过物理变化就可以得到钾单质
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备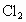
D.利用潮汐发电是将化学能转化为电能
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com