
【题目】某课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,采用了不同的实验方法(装置如图所示)。
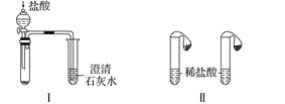

(1)根据上图Ⅰ、Ⅱ所示实验,能够达到实验目的的是(填装置序号)____。
(2)图Ⅲ所示实验能够鉴别这两种物质,其反应的化学方程式为_______。
(3)图Ⅳ不仅能鉴别碳酸钠和碳酸氢钠,同时又能验证碳酸钠和碳酸氢钠的稳定性,则试管B中装入的物质为__________,实验过程中的现象为________。
【答案】Ⅱ 2NaHCO3![]() Na2CO3+CO2↑+H2O 碳酸氢钠 a中石灰水变浑浊,b中石灰水不变浑浊
Na2CO3+CO2↑+H2O 碳酸氢钠 a中石灰水变浑浊,b中石灰水不变浑浊
【解析】
(1)碳酸钠和盐酸反应分两步进行,盐酸和碳酸钠、碳酸氢钠反应都生成二氧化碳,二氧化碳能使澄清的石灰水变浑浊;
(2)碳酸氢钠在加热条件下能分解生成碳酸钠和水、二氧化碳;
(3)根据碳酸氢钠不稳定的性质可知,为便于比较,B中受热温度低而易分解。
(1)Ⅰ装置反应现象相同;Ⅱ装置,向碳酸钠溶液中滴加盐酸先没有气体生成,随着盐酸的不断滴加,后产生气泡,向碳酸氢钠溶液中滴加盐酸立即产生气泡,所以能够达到实验目的是Ⅱ;
(2)III中碳酸氢钠在加热条件下能分解生成碳酸钠和水、二氧化碳,碳酸钠不能,反应的方程式为2NaHCO3![]() Na2CO3+CO2↑+H2O;
Na2CO3+CO2↑+H2O;
(3)碳酸钠直接加热在较高的温度下不分解,而碳酸氢钠不直接加热在较低的温度下就能分解,可以说明碳酸氢钠不稳定、碳酸钠稳定,否则不能证明两者的稳定性的强弱关系。所以试管B中装入的固体是碳酸氢钠,观察到现象为a中石灰水变浑浊,b中石灰水不变浑浊。


 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源: 题型:
【题目】在实验室中用二氧化锰跟浓盐酸反应制备干燥纯净的氯气。
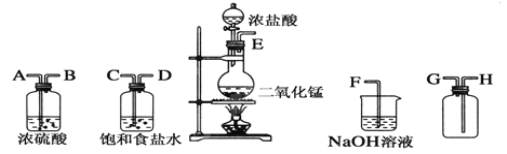
(1)连接上述仪器的正确顺序(填各接口处的字母):E接________;__________接__________;________接________;__________接F。
(2)装置中,饱和食盐水的作用是_____________________________________;浓硫酸的作用是________________________________________________。
(3)化学实验中检验是否有Cl2产生的常用方法是_________________________。
(4)写出下列反应的化学方程式:
①气体发生装置中的反应:_____________________________________。
②NaOH溶液中发生的反应:________________________________________。
(5)工业上用氯气制取漂白粉的化学反应方程式为__________________,漂白粉用于漂白、杀菌的原理用化学方程式表示为____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电化学应用广泛。请回答下列问题:
(1)自发进行的氧化还原反应可以设计成原电池。若电池放电时的反应式为:2Cu+2H2SO4+O2= 2CuSO4+2H2O,该电池的负极材料为_________;正极的电极反应式为__________________。
(2)燃料电池和二次电池的应用非常广泛。
①如图为甲烷燃料电池的示意图,电池工作时,b极的电极名称为_______;负极的电极反应式为____________;

②铅蓄电池为生活中常用的二次电池。放电时的反应为:PbO2 + Pb+ 2H2SO4 === PbSO4 + 2H2O,铅蓄电池负极的电极反应式为__________;充电时,铅蓄电池的PbO2极应与外加直流电源的__极相连,PbO2极的电极反应式为_________。
(3)以铅蓄电池为电源精炼粗铜(含Fe、Pb、Ag、Au及其他不反应质)时,以硫酸铜溶液为电解质溶液,粗铜做_____极;精炼一段时间后,当阴极增重128 g时,铅蓄电池参加反应的硫酸的物质的量为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下的可逆反应CO(g)+2H2(g)![]() CH3OH(g) △H <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )
CH3OH(g) △H <0,按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如右图所示。下列说法正确的是 ( )

A. 温度:T1 < T2 3
B. 正反应速率:ν(a)>ν(c); ν(b)>ν(d)
C. 平衡常数: K(a) =K(c) ; K(b) >K(d)
D. 平均摩尔质量:M(a)<m(c); m(b)>M(d)</m(c); m(b)>
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用下图所示联合装置制备金属钛,下列叙述错误的是( )
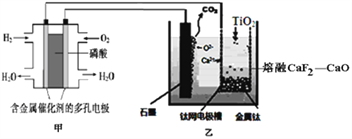
A. 甲装置工作过程中pH增大
B. 乙装置中石墨电极反应式为C-4e-+2O2-=CO2↑
C. 甲装置中通入O2的电极反应式为:O2+4e-+4H+=2H2O
D. 若不考虑装置的损失,制备24.0g金属钛,需要消耗氢气22.4L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,若电解5 min时铜电极质量增加2.16g,试回答:
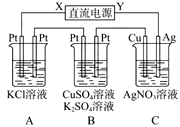
(1)电源电极X名称为______。
(2)pH变化:A ______,B ______,C ______。
(3)通电5min时,B中共收集224mL气体(标准状况),溶液体积为200mL,(设电解前后溶液不变)则通电前CuSO4溶液的物质的量浓度为 ______。
(4)若A中KCl溶液的体积也是200mL,电解后,溶液的pH是 ______(设前后体积无变化)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于铝的叙述中,不正确的是( )
A. 铝是地壳里含量最多的金属元素
B. 在常温下,铝不能与氧气反应
C. 铝是一种比较活泼的金属
D. 在化学反应中,铝容易失去电子,是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. CH4、CCl4都是含有极性键的非极性分子
B. NH3、CO、CO2都是极性分子
C. HF、HCI、HBr、HI的稳定性依次增强
D. CS2、H2O、C2H2都是直线型分子
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com