
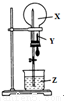
某同学准备利用下图进行喷泉实验,已知圆底烧瓶内充满X气体,胶头滴管内装有少量Y液体,烧杯内装有足量Z液体,下列组合能进行喷泉实验且最终液体一定能充满整个烧瓶的是( )
X气体 | Y试剂 | Z试剂 | |
A. | NO2 | H2O | H2O |
B. | NH3 | CCl4 | CCl4 |
C. | HCl | 饱和食盐水 | 水 |
D. | NO2和O2 | H2O | H2O |
 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源:2015-2016学年福建省高二上学期期中测试化学试卷(解析版) 题型:选择题
为了研究影响化学反应速率的因素,甲、乙、丙、丁四位学生分别设计了如下四个实验,你认为不正确的是
A.100 mL 2 mol·L-1的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
B.将相同大小、形状的铝条与稀硫酸和浓硫酸反应时,稀硫酸产生氢气快
C.将氢气和氯气的混合气体分别放在冷暗处和强光照射下,会发现光照下有氯化氢生成
D.两支试管中分别加入相同浓度相同体积的双氧水,其中一支试管再加入少量二氧化锰,产生氧气的快慢不同
查看答案和解析>>
科目:高中化学 来源:2016届江苏省淮安市高三上学期10月阶段测化学试卷(解析版) 题型:选择题
已知NH4CuSO3与足量的稀硫酸混合微热,产生下列现象:①有红色金属生成;②有刺激性气味气体产生;③溶液呈蓝色。据此判断下列说法正确的是
A、反应中硫酸作氧化剂
B、NH4CuSO3中S元素被氧化
C、刺激性气味的气体是氨气
D、1 mol NH4CuSO3完全反应转移0. 5 mol电子
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第四次考试化学试卷(解析版) 题型:填空题
I.元素X、Y、Z、M、N均为短周期主族元素,且原子序数依次增大。已知Y原子最外层电子数与核外电子总数之比为3:4,M原子的最外层电子数与次外层电子数之比为3 :4,且M原子的质子数是Y原子的2倍;N-、Z+、X+离子半径逐渐减小;化合物XN常温下为气体,请回答下列问题:
(1)写出Y、Z、N按原子个数之比1 :1:1形成的化合物的电子式_______________。
(2)写出由X、Y、Z、M、N中某些原子形成的18电子分子和18电子离子发生氧化还原反应的离子方程式:_________________。
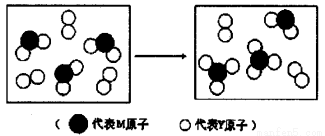
(3)上图表示由上述两种元素组成的气体分子在一定条件下的密闭容器中充分反应前后的转化关系,请写出该转化过程的化学方程式:________________。
Ⅱ.A、B、C、D是原子序数均小于20的四种元素。A与B同主族,且能形成BA2、BA3的型分子。B、C、D所形成的简单离子电子层结构相同,且B、C、D离子半径依次减小。请回答下列问题:
(4)D元素在元素周期表中的位置是_____。B与D所形成的化合物的化学键类型为______。
(5)将C单质的水溶液滴加到B与D所形成化合物的水溶液中,其反应的离子方程式为_。
查看答案和解析>>
科目:高中化学 来源:2016届江西省南昌市高三上学期第三次考试化学试卷(解析版) 题型:选择题
亚硝酸钠(有毒性,市场上很易与食盐混淆)是一种常见的工业用盐,广泛用于物质合成、金属表面处理等,物理性质与NaCl极为相似。相关化学性质如下图所示,下列说法不正确的是
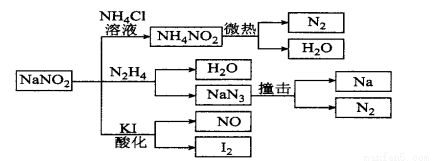
A.NaNO2稳定性大于NH4 NO2
B.NaNO2与N2 H4反应中,NaNO2是氧化剂
C.可用KI-淀粉试纸和食醋鉴别NaNO2和NaCl
D.分解NaN3盐每产生1 mol N2转移6 mol e一
查看答案和解析>>
科目:高中化学 来源:2016届江西上高第二中学高三12月月考理科综合化学试卷(解析版) 题型:选择题
现有短周期元素X、Y、Z、M,X、Y位于同主族,Z、M位于同主族,Y、Z位于同周期,X与Z、M都不在同一周期,Z的核电荷数是M的2倍。下列说法正确的是
A.简单阳离子的氧化性:Y>X
B.气态氢化物的稳定性:Z>M
C.等浓度X2Z与Y2Z的溶液中,水的电离程度:X2Z>Y2Z
D.简单离子半径由大到小的顺序是:Z>M>Y
查看答案和解析>>
科目:高中化学 来源:2016届黑龙江哈尔滨师大附中高三上学期期中考试化学试卷(解析版) 题型:推断题
A~H均为短周期元素,A~F在元素周期表中的相对位置如图所示,G与其它七种元素不在同一周期,H是短周期中原子半径最大的主族元素。由B、G组成的气态化合物甲水溶液呈碱性。
A | B | C | |
D | E | F |
请回答下列问题:
(1)写出甲的电子式 ,实验室制取气体甲的化学方程式为 。
(2)B、C、G个数比为1:1:5形成的化合物的化学键类型为 。
A.离子键 B. 极性键 C. 非极性键
(3)请用电子式表示AE2的形成过程 。
(4)用离子符号表示C、E、F、H四种离子的半径由大到小的顺序 。
(5)用一个离子方程式解释A比D非金属性强的原因 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:实验题
NH3是重要的化工原料。
(1)用NH4Cl和Ca(OH)2制备NH3,反应发生、气体收集和尾气处理装置依次为 。
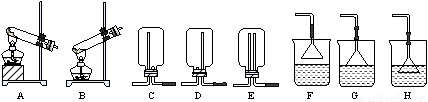
(2)某学生用下图装置对NH3与NaClO的反应进行实验探究:
操作 | 现象 |
| 液面上方出现白雾 |
资料:氨和次氯酸钠溶液反应能生成肼。肼常温下是无色液体,沸点:113℃,与水混溶,它的水溶液是一种二元弱碱。
①向水中持续通入NH3,未观察到白雾。推测现象中的白雾由N2H4小液滴形成,进行实验:用湿润的红色石蕊试纸检验白雾,试纸变蓝。该实验不能判断白雾中含有N2H4,理由是 。
②进一步实验确认了A中生成了N2H4。写出A中反应的化学方程式(N2不参与反应) ;此反应中若有5.6L氨气(标准状况下)参加反应,则转移电子的数目为_______。
查看答案和解析>>
科目:高中化学 来源:2015-2016浙江宁波效实中学高二上期中考试化学试卷卷(解析版) 题型:选择题
室温下,有关下列四种溶液的叙述正确的是(忽略溶液混合的体积变化)
① | ② | ③ | ④ | |
pH | 12 | 12 | 2 | 2 |
溶液 | 氨水 | 氢氧化钠溶液 | 醋酸 | 盐酸 |
A.在①、②中分别加入氯化铵晶体,两溶液的pH值均增大
B.分别将等体积的①和②加水稀释100倍,所得溶液的pH:①>②
C.把①、④两溶液等体积混合后所得溶液显酸性
D.将溶液②和溶液③等体积混合,混合后所得溶液pH=7
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com