

| A、用锌粒与稀硫酸制取并收集H2 |
| B、用生石灰和浓氨水制取并收集NH3 |
| C、用少量MnO2和H2O2制取并收集O2 |
| D、用浓硫酸和浓盐酸制取并收集HCl |


 黎明文化寒假作业系列答案
黎明文化寒假作业系列答案 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案科目:高中化学 来源: 题型:
| A、1.6g由氧气和臭氧组成的混合物中含有氧原子的数目为0.1NA | ||
B、标准状况下,1L戊烷充分燃烧后生成的气态产物的分子数为
| ||
| C、pH=13的NaOH溶液中含有的OH-为0.1mol | ||
| D、在过氧化钠与水的反应中,每生成0.1mol氧气,转移电子的数目为0.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清的石灰水跟盐酸反应:H++OH-═H2O |
| B、铁和稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
| C、NaHCO3溶液与NaOH溶液反应:OH-+HCO3-=CO32-+H2O |
| D、金属钠跟水反应:Na+2H2O═Na++2OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验方案 | 预测现象 | 预测依据 |
| 操作1:向2mL Na2CO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 有白色沉淀 | Na2CO3溶液中的CO32-浓度较大,能与CaCl2发生反应Ca2++CO32-=CaCO3↓. |
| 操作2:向2mL NaHCO3溶液中滴加1mL 0.5mol?L-1CaCl2溶液 | 无白色沉淀 | NaHCO3溶液中的CO32-浓度很小,不能与CaCl2反应. |
查看答案和解析>>
科目:高中化学 来源: 题型:
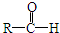 +R′-CH2-CHO→
+R′-CH2-CHO→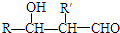 (其中R、R′为烃基,也可以是氢原子)产物不稳定,受热易脱水而生成不饱和醛.
(其中R、R′为烃基,也可以是氢原子)产物不稳定,受热易脱水而生成不饱和醛.
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、能使酸性高锰酸钾溶液褪色是因为H2SO3的漂白性 |
| B、H2SO3在空气中容易变质,成为SO2 |
| C、溶液中存在的微粒只有H+和SO32- |
| D、能与NaOH溶液发生复分解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com