
下列结论是从某同学的作业本上摘录的,其中你认为肯定正确的是( )
①微粒半径:S2->Cl>S>F
②氢化物的稳定性:HF>HCl>H2S>H2Se
③还原性:S2->Cl->Br->I- ④氧化性:Cl2>S>Se>Te
⑤酸性:H2SO4>HClO4>H2SeO4 ⑥得电子能力:F>Cl>S>Se
A.①⑤ B.①③④ C.②④⑥ D.⑥
科目:高中化学 来源: 题型:
元素周期律和周期表,揭示了元素之间的内在联系,反映了元素性质与它的原子结构的关系,在哲学、自然科学、生产实践各方面都有重要意义。下表为元素周期表的一部分,请参照元素①~⑧在表中的位置,回答下列问题:
 |

(1)这8种元素中金属性最强的元素是______(填元素符号或化学式,下同),元素最高价氧化物对应的水化物中酸性最强的酸是______;
(2)元素⑧的最高价氧化物对应的水化物与氢氧化钠反应的离子方程式是_________;
(3)③、⑤、⑦三种元素按原子半径由大到小的顺序排列为___________;
 (4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(4)①、④、⑤中的某些元素可形成既含离子键又含共价键的离子化合物,写出两种化合物的电子式______________,______________。若用球棍模型表示①和④形成的化合物的分子结构,应该是___________。
(5)w是第四周期与③同主族的元素。据此推测w不可能具有的性质是
A.最高正化合价为+5价 B.气态氢化物比NH3稳定
C.最高价氧化物的水化物的酸性比硝酸弱 D.单质在常温下可与氢气化合
(6)由表中元素形成的常见物质X、Y、Z、M、N可发生以下反应:
|
|

X溶液与Y溶液反应的离子方程式_______,M中阳离子的鉴定方法____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知反应A+B=C+D的能量变化如图所示,下列说法正确的是( )
A.该反应为放热反应
B.该反应为吸热反应
C.反应物的总能量高于生成物的总能量
D.该反应只有在加热条件下才能进行

查看答案和解析>>
科目:高中化学 来源: 题型:
根据如图所示图像,写出反应的热化学方程式并回答下列问题:

(1)反应过程①的热化学方程式为:
_____________________________________________________。
(2)反应过程②的热化学方程式为:
_____________________________________________________。
(3)Q与Q1的关系:Q______Q1(填“<”、“>”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
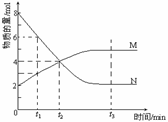
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述正确的是( )
A.反应的化学方程式:2M  N
N
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
已知1 molCO气体完全燃烧生成CO2 气体放出283 kJ热量;1 mol氢气完全燃烧生成液态水放出286 kJ热量; 1 molCH4气体完全燃烧生成CO2气体和液态水放出890 kJ热量。
(1) 写出表示氢气燃烧热的热化学方程式 。
(2) 若 1 molCH4气体完全燃烧生成CO2气体和水蒸气,放出热量 为 890 kJ( 填“>”、 “<”、“= ”)。
(3) 若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水时,则放出热量(Q)的取值范围是 。
(4) 若将a molCH4、CO和H2的混合气体完全燃烧,生成 CO2气体和液态水,且CO2和水的物质的量相等时,则放出热量(Q)的的取值范围是:
。
查看答案和解析>>
科目:高中化学 来源: 题型:
某甲酸溶液中含有甲醛,用下列方法可以证明的是 ( )
A.加入足量的新制氢氧化铜并加热煮沸,有砖红色的沉淀
B.加入过量的氢氧化钠充分反应后的溶液能发生银镜反应
C.将试液进行酯化反应后的混合液能发生银镜反应
D.加入足量氢氧化钠后,蒸馏出的气体通入新制的氢氧化铜悬浊液加热有砖红色沉淀
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com