
【题目】(化学—选修5:有机化学基础)
绿原酸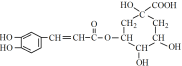 是一种抗氧化药物,存在下图转化关系。
是一种抗氧化药物,存在下图转化关系。
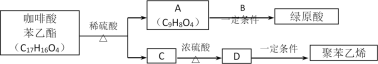
(1)绿原酸中的含氧官能团有:__________________________________。
(2)B的分子式是_____________________。
(3)C的氧化产物能发生银镜反应,则C的名称________________,写出C→D的化学方程式是______________________。
(4)咖啡酸苯乙酯的结构简式是___________________________________。
(5)F是A的同分异构体。F分别与碳酸氢钠溶液或新制Cu(OH)2反应产生气体或红色沉淀;苯环上只有两个取代基,且核磁共振氢谱表明该有机物中有8种不同化学环境的氢。
①符合上述条件的F有________种可能的结构。
②若F还能与NaOH在常温下以物质的量之比1∶2完全反应,其化学方程式是______(任写1个)。
【答案】羟基、羧基、酯基 C7H12O6 苯乙醇 ![]()
![]() 6
6 ![]()
(或 ![]() )
)
【解析】
咖啡酸苯乙酯(C17H16O4)在稀硫酸条件下发生水解反应生成A(C9H8O4)与C,C在浓硫酸、加热条件下生成D,D一定条件下生成聚苯乙烯,故D为![]() ,C的氧化产物能发生银镜反应,C为醇,故C为
,C的氧化产物能发生银镜反应,C为醇,故C为![]() ,A中含有-COOH,结合绿原酸的结构可知,A为
,A中含有-COOH,结合绿原酸的结构可知,A为![]() ,故B为
,故B为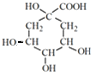 ,据此答题。
,据此答题。
(1)根据绿原酸的结构判断含氧官能团;
(2)根据B的结构简式书写其分子式;
(3)C是苯乙醇,C→D是![]() 发生消去反应生成
发生消去反应生成![]() ;
;
(4))咖啡酸苯乙酯的结构简式是![]() ;
;
(5)F是![]() 的同分异构体,F可以与碳酸氢钠溶液反应产生气体,分子中含有-COOH,也可以与新制Cu(OH)2反应产生砖红色沉淀,含有-CHO,F的苯环上只有两个取代基,结合A的结构书写符合上述条件F的结构简式。
的同分异构体,F可以与碳酸氢钠溶液反应产生气体,分子中含有-COOH,也可以与新制Cu(OH)2反应产生砖红色沉淀,含有-CHO,F的苯环上只有两个取代基,结合A的结构书写符合上述条件F的结构简式。
(1)根据绿原酸的结构可知,绿原酸中含氧官能团有:酯基、羟基、羧基,
故答案为:羟基、羧基、酯基。
(2)由书写分析可知,B为 ,其分子式为C7H12O6,
,其分子式为C7H12O6,
故答案为:C7H12O6。
(3)C→D是![]() 发生消去反应生成
发生消去反应生成![]() ,反应方程式为:
,反应方程式为:![]() ,
,
故答案为:![]() 。
。
(4)由上述分析可以知道,咖啡酸苯乙酯的结构简式是![]() ,故答案为:
,故答案为:![]() 。
。
(5)①F是![]() 的同分异构体,F可以与碳酸氢钠溶液反应产生气体,分子中含有-COOH,也可以与新制Cu(OH)
的同分异构体,F可以与碳酸氢钠溶液反应产生气体,分子中含有-COOH,也可以与新制Cu(OH)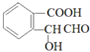 (邻、间、对三种)
(邻、间、对三种)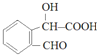 (邻、间、对三种),共有6种。
(邻、间、对三种),共有6种。
故答案为:6。
②若F还能与NaOH在常温下以物质的量之比1:2完全反应,则F为含有酚羟基、-COOH,则F为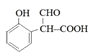 ,反应方程式为:
,反应方程式为:![]() ,
,
(或![]() ),
),
故答案为:![]()
(或![]() )。
)。


科目:高中化学 来源: 题型:
【题目】我国科学家通过测量SiO2中26 Al和10 Be两种元素的比例来确定“北京人”的年龄,这种测量方法叫铝铍测年法。下列关于26 Al和10 Be的说法不正确的是( )
A. 10 Be和9 Be是中子数不同、质子数相同的不同原子
B. 10 Be原子核内的中子数比质子数多
C. 5.2g 26 A13+中所含的电子数约为1.2![]() 1023
1023
D. 26AI和26 Mg的质子数、中子数和核外电子数都不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学内容填空:
Ⅰ.化学反应 2A+B2C;△H<0达到化学平衡时,根据以下条件改变填空:
(1)若A、B、C都是气体,且C为有色气体.
①使密闭容器体积增大,A的转化率_______;(填增大、减小、不变)
②如果升高温度,平衡混合物的颜色______;(填加深、变浅、不变)
(2)若A、C为气体,B为固体;
①加压,则A的体积分数________;(填增大、减小、不变)
②增加B的量,A的转化率_______.(填增大、减小、不变)
Ⅱ.(1)H2S溶于水的电离方程式为________________________。向H2S溶液中加入NaOH固体时,c(H+)_________,c(S2-)__________。(填增大、减小或不变)
(2) 下列物质能导电且属于电解质的是________(填序号)。
A.铁 B.盐酸 C.氯化钠晶体 D.熔融氢氧化钠
(3)23g C2H5OH(l)完全燃烧生成CO2(g)和H2O(l),放出683.4 kJ热量,写出该反应的热化学方程式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,10.0mL 下列气态有机物在 50.0mL O2中充分燃烧后,将生成的气体混合物通过足量浓硫酸,剩余35.0mL 的气体混合物(反应前后压强相等),则该有机物可能是
A. C3H8OB. C2H6O2
C. C4H10O2D. C6H6
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应4NH3(g)+5O2(g)===4NO(g)+6H2O(g)在2 L密闭容器中进行1分钟后,NH3减少了0.12 mol,则平均每秒钟浓度变化正确的是( )
①NO:0.001 mol·L-1 ②H2O:0.002 mol·L-1
③NH3:0.002 mol·L-1 ④O2:0.001 25 mol·L-1
A. ①④ B. ②③ C. ③④ D. ①②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酰氯(SO2Cl2)常作氯化剂或氯磺化剂,用于制作药品、染料、表面活性剂等。其部分性质如下表:
物质 | 熔点/℃ | 沸点/℃ | 其它性质 |
SO2Cl2 | -54.1 | 69.1 | ①易水解产生大量白雾 ②易分解:SO2Cl2 |
回答下列问题:
I.已知:SO2(g)+Cl2(g) ![]() SO2Cl2(l) ΔH = 97.3 kJ·mol-1。催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):
SO2Cl2(l) ΔH = 97.3 kJ·mol-1。催化合成硫酰氯的实验装置如下图 (夹持仪器已省略):

(1)仪器B的名称是____________,冷却水的进口为________(填“a”或“b”)。
(2)装置D除干燥气体外,另一作用是______________________。若缺少D,则硫酰氯会水解,该反应的化学方程式为_________________________________________。
(3)实验室用二氧化锰和浓盐酸反应制取氯气,写出其反应的离子方程式:__________________________________
(4)C处U形管中碱石灰的作用除吸收多余SO2、Cl2,防止污染外;还有_______________________。
II.在氯磺酸中加入四氯化锡加热煮沸,使氯磺酸分解,可用于制取少量硫酰氯。化学方程式为:2ClSO3H![]() H2SO4+SO2Cl2,此法得到的产品中混有硫酸。
H2SO4+SO2Cl2,此法得到的产品中混有硫酸。
(5)①从分解产物中分离出硫酰氯的方法是_____________。
②请设计实验方案检验产品中硫酸的存在(可选试剂:稀盐酸、稀硝酸、BaCl2溶液、蒸馏水、石蕊溶液):取适量产品,充分___________后,加水稀释__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如图所示的转化关系,水和部分产物已略去。

已知:①X和Z是两种透明、不溶于水的坚硬固体,其中Z无固定熔点,是现代建筑不可缺少的装饰和采光材料;②无色气体A是引起温室效应的主要气体;
③B、D均为难溶于水的白色固体;④高纯度的F是使用最广泛的半导体材料。
据此回答下列问题:
(1)Z的名称是________,工艺师在Z表面刻蚀花纹图案需用的试剂为________(填名称)。
(2)由X、Y制F的化学方程式为________________________,此反应中Y作________剂(填“氧化”或“还原”)。
(3)转化①的化学方程式为________________________;转化②(A少量)的离子方程式为______________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com