
| A、富含N、P元素的生活用水可以直接用来灌溉农田 |
| B、淀粉、纤维素、蛋白质、葡萄糖都是天然高分子化合物 |
| C、“地沟油”虽然对人体有害,但对“地沟油”进行分馏可制得汽油、煤油,达到变废为宝的目的 |
| D、蛋白质、油脂、蔗糖都能水解,但水解产物都不相同 |


科目:高中化学 来源: 题型:
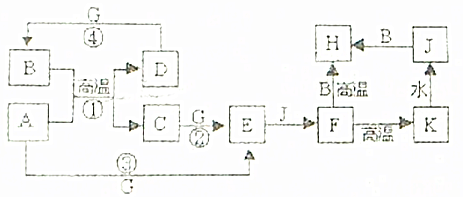
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、X、Y、Z分子中均含有2个手性碳原子 |
| B、X、Y、Z均能与FeCl3溶液发生显色反应 |
| C、1mol Y最多能消耗2molH2 |
| D、1molZ与NaOH溶液反应最多消耗3molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、该反应的反应热△H=E1-E2 |
| B、a、b分别对应有催化剂和无催化剂的能量变化 |
| C、催化剂能降低反应的活化能 |
| D、催化剂能改变反应的焓变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将城市的大型电镀工厂改建在农村,既促进农村经济发展又减轻城市用水污染 | ||||
| B、可吸入颗粒(例如硅酸盐粉尘)形成气溶胶,对人类健康危害极大 | ||||
| C、核裂变是一种化学变化 | ||||
D、核电站泄露的
|
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)=c(CH3COO-) |
| B、c(CH3COO-)+c(CH3COOH)=0.1 mol?L-1 |
| C、由水电离出来的c(OH-)=1.0×10-11 mol?L-1 |
| D、往该溶液中加入等体积的水,pH值变大 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述I | 陈述II |
| A | 常温下铁与浓硫酸不反应 | 可用铁槽车密封运送浓硫酸 |
| B | NaHCO3溶于水完全电力 | NaHCO3是强电解质 |
| C | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| D | H2O2、SO2能使酸性KMnO4溶液褪色 | H2O2表现还原性,SO2表现漂白性 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学反应中的热效应
化学反应中的热效应| 实验次数 | 起始温度t1/℃ | 终止温度t2/℃ | |
| 盐酸 | NaOH溶液 | ||
| 1 | 20.2 | 20.3 | 23.7 |
| 2 | 20.3 | 20.5 | 23.8 |
| 3 | 21.5 | 21.6 | 24.9 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com