
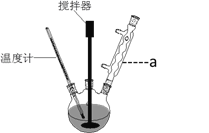
����Ŀ����˹ƥ�ֵ��Ʊ�װ�úͷ�Ӧԭ�����£�
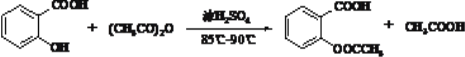
��֪������(CH3C0)2O��ˮ�лᷢ��ˮ�ⷴӦ�������ᡣ
ʵ�鲽�裺
�ٿ���ˮԡ���²۵ĵ�Դ��ʹˮԡ�¶ȿ�����85��-90�档
��������ƿ�м���5gˮ���ᣬ14ml��15g��������(CH3C0)2O��1.8mlŨ���ᡣ
����ˮԡ�У����跴Ӧ15min����ȴ�����£���ƿ�м���70mlˮ����������5min���ٷ�����ˮԡ�о���5��10min��������飬�ڱ�ˮԡ�о���10��20min����ȴ�ᾧ�����ˣ���������ˮϴ��2�Ρ�
�ܽ��������250ml�ձ��У�������70ml����̼��������Һ�����赽������̼�ų�Ϊֹ�����˳�ȥ�ۺ�����塣
�ݽ���Һ����250ml�ձ��У��߽������������18%���ᣬֱ��PHֵΪ1.5���ձ������ˮԡ����ȴ��ֱ���ᾧ��ȫ����ճ��ˣ���������ˮϴ�Ӷ��Σ��ôֲ�Ʒ��
�ֲ�Ʒ����150ml�ձ��У�����20ml��ˮ�Ҵ������裬�������ȣ�ֱ�������ܽ⣬�ټ���40mlˮ���������о��ã��ٷ����ˮԡ����ȴ��ֱ���ᾧ��ȫ����ճ��ˣ���������ˮ�Ҵ�-ˮ��1:2��v/v����Һϴ�ӣ���ɣ��ò�Ʒ��������������ʡ�
�ش��������⣺
��1������a������Ϊ_________________
��2����Ӧ����������ˮ��ԭ����__________________________________������Ũ�����Ŀ����______________________________________��ˮԡ���ȵ�Ŀ����__________________________
��3����ʵ�麬��������Ԫ����һ����Ԫ���ĸ�����Ľṹ��ʽΪ__________________��
��4������70ml����̼��������Һ��Ŀ����__________________________________����̼�����ƻ�Ϊ�������ƽ�ʹ��Ʒ��________________________����ʧ��
��5������Һ�߽������������18%����������______________________________��ԭ����
��6��ˮ��������ڸ����������̺Ͳ�����ؽᾧ�����б���ȥ������ˮ��������ķ�����____________________________________________________________________��
���𰸡� ���������� �Է�ֹ������ˮ��ת�������� ������ ʹ���Ⱦ��ȣ����ڿ����¶� 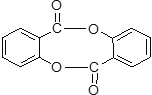 ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ���߷��Ӹ�������� ����ˮ�� ǿ�������� ��������Ʒ����ʢ������ˮ���Թ��У�����FeCl3��Һ���۲�������ɫ����
ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ���߷��Ӹ�������� ����ˮ�� ǿ�������� ��������Ʒ����ʢ������ˮ���Թ��У�����FeCl3��Һ���۲�������ɫ����
����������1������aΪ����������װ�ã�����Ϊ���������ܣ���ȷ�������������ܡ�
��2��������(CH3C0)2O��ˮ�лᷢ��ˮ�ⷴӦ�������ᣬ��˷�Ӧ������Ҫ���ָ�����ˮ��������Ӧ��Ҫ��һ���������½��У�Ũ�������������¶Ȳ�����100��ʱ��һ�����ˮԡ���ȣ�������ʹ��Ӧ�����Ⱦ��ȣ����ڿ����¶ȣ���ȷ��: ��ֹ������ˮ��ת���������������ʹ���Ⱦ��ȣ����ڿ����¶ȡ�
��3��2���ӵ�ˮ������䷢��ȡ����Ӧ���������ṹ��ʽΪ ����ȷ�𰸣�
����ȷ�𰸣� ��
��
��4��ʵ�����ò�ƷΪ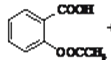 ��������Ϊ
��������Ϊ ����˼���70ml����̼��������Һ��Ŀ����ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ��ﵽ��߷��Ӹ�������룻�����̼�����ƻ�Ϊ�������ƣ����ò�Ʒ
����˼���70ml����̼��������Һ��Ŀ����ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ��ﵽ��߷��Ӹ�������룻�����̼�����ƻ�Ϊ�������ƣ����ò�Ʒ �ܹ�����ˮ�⣬���²�Ʒ��ʧ����ȷ�𰸣�ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ���߷��Ӹ�������룻����ˮ�⡣
�ܹ�����ˮ�⣬���²�Ʒ��ʧ����ȷ�𰸣�ʹ��Ʒת��Ϊ������ˮ�����Σ�������ۺ��ﲻ������NaHCO3��Һ���Ӷ���߷��Ӹ�������룻����ˮ�⡣
��5������Һ�߽������������18%���ᣬ����˹ƥ�ֵĿ�����������ת��Ϊ��˹ƥ��,�Ӷ��ﵽ�ᴿ��Ŀ�ģ��÷�Ӧ������ǿ���������ԭ������ȷ�𰸣�ǿ�������ᡣ
��6��ˮ����Ľṹ�к����Ȼ��ͷ��ǻ�����˿��Բ��õμ��Ȼ�����Һ�۲��л����Ƿ��ɫ���м��飬�������£���������Ʒ����ʢ������ˮ���Թ��У�����FeCl3��Һ���������ɫ���֣���Ʒ�о�û��ˮ�����ȷ�𰸣���������Ʒ����ʢ������ˮ���Թ��У�����FeCl3��Һ���۲�������ɫ���֡�


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NAΪ�����ӵ�������ֵ�������й�������ȷ����
A. �ں�A13+����ΪNA��A1C13��Һ�У�C1-����Ϊ3NA
B. ��״���£�5.6L CO2�к��еĹ��õ��Ӷ���Ϊ0.5NA
C. Na2O2��������CO2��Ӧ����0.1mol O2��ת�Ƶĵ�����Ϊ0.2NA
D. �����£�56g��ƬͶ������ŨH2SO4�У���ַ�Ӧ������NA��SO2����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������и�װ��ͼ�������У�������ǣ�
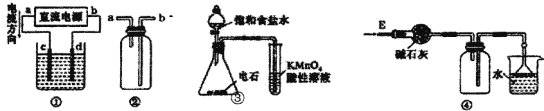
A. װ�â�������ⱥ��ʳ��ˮ��c�缫������������ʹʪ��ĵ���KI��ֽ����
B. װ�âڿ������ռ�H2��NH3��Cl2��HCl��NO2
C. װ�âۼ����Ȳ�Ļ�ԭ�ԣ�ʵ�������ɱ���ʳ��ˮ���ʯ����Ȳ�������Ļ���������Ȳ�⣬������H3P ��H2S���������壩
D. װ�âܿ����ڸ���ռ������������ն���İ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ѧ������Ф���2005��ŵ������ѧ������������ϩ�����̼̼˫���ᱻ��ɢ�����飬�γ��·��ӣ����ֹ��̱�����Ϊϩ�����ֽⷴӦ���ù��̿ɷ����ڲ�ͬϩ�����Ӽ䣬Ҳ�ɷ�����ͬ��ϩ�����Ӽ䣩��
�磺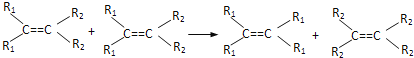
������л���![]() ����ϩ���ĸ��ֽⷴӦʱ�����������ɵIJ�����( )
����ϩ���ĸ��ֽⷴӦʱ�����������ɵIJ�����( )
A. ![]() B.
B. ![]() C. CH2= CHCH3 D.
C. CH2= CHCH3 D. ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(Al2O3) �͵����裨Si3N4���������ĸ��½ṹ�մɣ��ڹ�ҵ�����ͿƼ���������Ҫ��;��
��1��Al��NaOH��Һ��Ӧ�����ӷ���ʽΪ_____________________________________��
��2������ʵ���ܱȽ�þ�����Ľ�����ǿ������____________������ţ���
a���ⶨþ�����ĵ�����ǿ��
b���ⶨ�����ʵ���Ũ�ȵ�Al2(SO4)3��MgSO4��Һ��pH
c����0.1 mol/L AlCl3��0.1 mol/L MgCl2�мӹ���NaOH��Һ
��3�����ȷ��dz��õĽ���ұ������֮һ��
��֪��4Al (s)+3O2(g) =2Al2O3(s) ��H1 = -3352 kJ/mol
Mn(s)+ O2(g) =MnO2 (s) ��H2 = -521 kJ/mol
Al��MnO2��Ӧұ������Mn���Ȼ�ѧ����ʽ��_____________________________��
��4����ҵ���û�ѧ����������Ʊ������裬�䷴Ӧ���£�
3SiCl4(g) + 2N2(g) + 6H2(g) ![]() Si3N4(s) + 12HCl(g) ��H��0
Si3N4(s) + 12HCl(g) ��H��0
ij�¶Ⱥ�ѹǿ�����£��ֱ�0.3mol SiCl4(g)��0.2mol N2(g)��0.6mol H2(g)����2L�ܱ������ڣ�����������Ӧ��5min�ﵽƽ��״̬������Si3N4(s)��������5.60g��
��H2��ƽ����Ӧ������_________ mol��(L��min)��
������n(SiCl4) : n(N2) : n(H2) = 3 : 2 : 6��Ͷ����ȣ���������������������ϣ�SiCl4(g)��ת����Ӧ______�����������С�����䡱����
��5��298Kʱ��Ksp[Ce(OH)4]��1��10��29��Ce(OH)4���ܶȻ�����ʽΪKsp��_______________��
Ϊ��ʹ��Һ��Ce4��������ȫ������������Һ�е�c(Ce4+)С��1��10��5mol��L��1�������pHΪ______���ϡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Լ��У����ô����������Լ�ƿ�������
A.�����B.��������C.����D.ˮ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��A��B��C��ԭ��������������Ķ���������Ԫ�أ�����Ԫ��ԭ������֮��Ϊ35����C��ԭ��������A��2����A��B��C����Ԫ�صĵ������ʵ������¿ɷ�����ͼ��ʾ�ı仯������˵����ȷ����

A. �ס��ҡ����������ʵ�ˮ��Һ���Լ���
B. ���Ǽ����������������������
C. �ס��ҿ��ܶ���Ư���ԣ���Ư��ԭ����ͬ
D. ����ˮ��Һ�ڿ����г��ڷ��ã���Һ���ܻ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵���У���ȷ����
A. ���ڻ������ȷ�ӦB. �ϳ�ϴ�Ӽ�ȥ��ԭ�����������
C. ��������֮�以��ͬϵ��D. ����Ũ���᳣���²�������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ������ͼʾװ���Ʊ�KClO��Һ������KOH��Fe(NO3)3��Һ��Ӧ�Ʊ���Ч��ˮ��K2FeO4��

<��������>Cl2��KOH��Һ��20�����·�Ӧ����KClO���ڽϸ��¶���������KClO3��
K2FeO4������ˮ������ŨKOH��Һ����0�桫5���ǿ������Һ�н��ȶ���
��1������a�����ƣ�__________��װ��C������ƿ���ڱ�ˮԡ�е�Ŀ����_____________��
��2��װ��B���յ�������__________��װ��D��������___________________________��
��3��C�еõ�����KClO������ƿ�ϵĵ���ȡ�£����μ���KOH��Һ��Fe(NO3)3��Һ��ˮԡ���Ʒ�Ӧ�¶�Ϊ25�棬����1.5 h����Һ��Ϊ�Ϻ�ɫ(��K2FeO4)���÷�Ӧ�����ӷ���ʽΪ________________________���ټ��뱥��KOH��Һ�������Ϻ�ɫ���壬���ˣ��õ�K2FeO4�ֲ�Ʒ��
��4��K2FeO4�ֲ�Ʒ����Fe(OH)3��KCl�����ʣ����ᴿ����Ϊ��
�ٽ�һ������K2FeO4�ֲ�Ʒ�������3 mol/L KOH��Һ�С�
�ڹ��ˡ�
��________________________________________________________��������������
�ܽ��衢���á����ˣ����Ҵ�ϴ��2��3�Ρ�
������ո������и��
��5����ȡ�ᴿ���K2FeO4��Ʒ0.2200 g���ձ��У�����ǿ�����Ǹ�������Һ����Ӧ���ټ�ϡ���������Һ��ǿ���ԣ����250 mL��Һ��ȡ��25.00 mL������ƿ����0.01000 mol/L��(NH4)2Fe(SO4)2��Һ�ζ����յ㣬�ظ�����2�Σ�ƽ������(NH4)2Fe(SO4)2��Һ30.00 mL���漰��Ҫ��ӦΪ��Cr(OH)4����FeO42�� �� Fe(OH)3����CrO42����OH����2CrO42����2H+![]() Cr2O72����H2O��Cr2O72����6Fe2+��14H+ �� 6Fe3+��2Cr3+��7H2O�����K2FeO4��Ʒ�Ĵ���Ϊ____________��
Cr2O72����H2O��Cr2O72����6Fe2+��14H+ �� 6Fe3+��2Cr3+��7H2O�����K2FeO4��Ʒ�Ĵ���Ϊ____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com