
| A. | H2O2→H2O | B. | NH4+→NH3 | C. | Fe3+→Fe2+ | D. | CO→CO2 |
分析 必须加入还原剂才能实现,说明给予物质作氧化剂,在反应中得电子化合价降低,据此分析解答.
解答 解:A.该反应中O元素化合价由-1价变为-2价,双氧水作氧化剂,但不需要加入还原剂也能实现,如双氧水分解,故A不选;
B.该反应中N、H元素化合价不变,不需要发生氧化还原反应就能实现,故B不选;
C.该反应中Fe元素化合价由+3价变为+2价,则铁离子作氧化剂,需要还原剂才能实现,如Fe、Cu等,故C选;
D.C元素化合价由+2价变为+4价,所以CO作还原剂,需要氧化剂才能实现,如氧气等,故D不选;
故选C.
点评 本题以氧化还原反应为载体考查氧化剂、还原剂判断,为高频考点,明确元素化合价与物质性质关系是解本题关键,易错选项是A,注意自身发生氧化还原反应情况,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 金属铝溶于氢氧化钠溶液:Al+2OH-═AlO2-+H2↑ | |
| B. | 足量二氧化碳通入NaOH溶液:CO2+OH-═HCO3- | |
| C. | Cl2溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| D. | 向沸水中滴加饱和的氯化铁溶液:Fe3++3H2O═Fe(OH)3↓+3H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
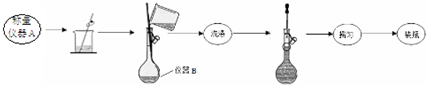
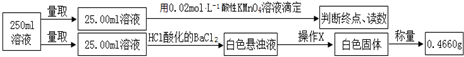
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 10.32 | 10.02 | 9.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若金属有剩余,在溶液中再滴入硫酸后,金属不溶解 | |
| B. | 若金属全部溶解,则溶液中一定含有Fe3+ | |
| C. | 若金属全部溶解,则溶液中一定含有Fe2+ | |
| D. | 若金属有剩余,不可能只有铁 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有单质参加或有单质生成的反应一定是氧化还原反应 | |
| B. | 氧化还原的本质是元素化合价的升降 | |
| C. | 失电子越多,该物质的还原性就越强 | |
| D. | 金属单质在化学反应中一定作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
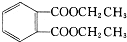 )是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法:
)是一种重要的工业塑化剂,其合成路线很多,下图就是其中的一种合成方法: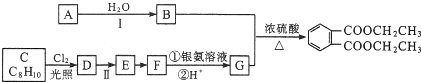
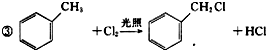
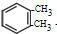 +2Cl2$\stackrel{光照}{→}$
+2Cl2$\stackrel{光照}{→}$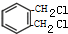 +2HCl.
+2HCl. .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 500 mL容量瓶,58.5 gNaCl | B. | 500 mL容量瓶,117 g NaCl | ||
| C. | 1 000 mL容量瓶,58.5 g NaCl | D. | 1 000 mL容量瓶,117 g NaC1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com