
科目:高中化学 来源: 题型:阅读理解
| 11.82g |
| 197g/mol |
| 11.82g |
| 197g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
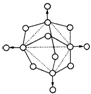 磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)
磷在空气中充分燃烧,生成X的分子结构如右图所示.图中实线表示化学键,圆圈表示原子(不考虑原子体积大小)查看答案和解析>>
科目:高中化学 来源: 题型:
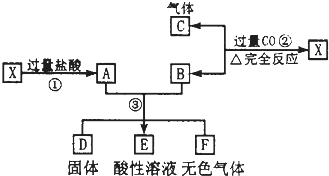 已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):
已知X为FeO和CuO的混合物,取两份等质量的X样品进行了①、②、③步实验,关系如图(其中固体D不溶于稀盐酸):查看答案和解析>>
科目:高中化学 来源:2011-2012学年安徽省省城名校高三第四次联考化学试卷 题型:选择题
在298K 1.0l×l05Pa下,将32g SO2通入750mL 1mol/L KOH溶液中充分反应.测得反应放出xkJ的热量。已知在该条件下,lmol SO2通入1 L 2mol/L KOH溶液中充分反应放出ykJ的热量。则SO2与KOH溶液反应生成KHSO3的热化学方程式正确的是( )
A.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(4x-y)kJ/mol
B.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(2x-y)kJ/mol
C.SO2(g)+KOH(aq)=KHSO3(aq) △H=-(2y-x)kJ/mol
D.2SO2(g)+2KOH(1)=2KHSO3(1) △H=-(8x-2y)kJ/mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com