
| A��25�棬101Kpaʱ�������ȼ����Ϊ890.3Kj?mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g��=CO2��g��+2H2O��l������H=-890.3Kj?mol-1 | |||
| B��500�桢30Mpa�£���0.5molN2��1.5molH2�����ܱյ������г�ַ�Ӧ����NH3��g��������19.3Kj�����Ȼ�ѧ����ʽΪ�� N2��g��+3H2��g��
| |||
| C���Ȼ�þ��Һ�백ˮ��Ӧ��Mg2++2OH-=Mg��OH��2�� | |||
| D��100Ml0.01moL/LϡNaOH��Һ��100Ml0.01moL/Lϡ���ᷴӦ���Ȼ�ѧ����ʽ�ɱ�ʾΪ��NaOH��aq��+CH3COOH��aq��=NaOOCCH3��aq��+H2O��l������H=-57.3Kj/mol |
| ���� |
| 500��30MPa |


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
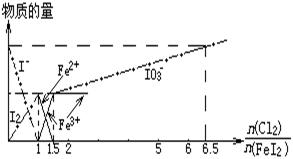
| A��I-��Fe2+��I2�Ļ�ԭ�Ժ�Cl2��Fe3+��I2�������Զ����μ�С |
| B����n(Cl2)/n(FeI2)==1.2ʱ�����ӷ���ʽΪ2Fe2++10I-+6Cl2==5I2+2Fe3++12Cl- |
| C����n(Cl2)/n(FeI2)==6.5ʱ����Һ��n(Cl-)/n(IO3-)==6.5 |
| D������Һ������䣬��Һ��pHʼ�ղ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A������ʯ��ˮ��ϡ���ᷴӦCa��OH��2+2H+=Ca2++2H2O | ||
| B����ˮ�����ᷴӦH++OH-=H2O | ||
C��ϡ����������������Һ��ӦBa2++2OH-+2H++SO
| ||
D��С�մ����ռ���Һ��ӦHCO
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����ʯ���ռ���Һ��Ӧ��SiO2+2OH-=SiO32-+H2O |
| B������ͨ��ˮ�У�Cl2+H2O=H++Cl-+ClO- |
| C�������ռ���Һ��2Al+2OH-+2H2O=2AlO2-+3H2�� |
| D������ʯ��ˮ������С�մ���Һ��ϣ�Ca2++OH-+HCO3-=CaCO3��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A����������Һ�м�������������ҺBa2++SO42-=BaSO4�� |
| B������ˮ��ӦNa+2H2O=Na++2OH-+H2�� |
| C��̼������Һ�м�����������CO32-+2H+=CO2��+H2O |
| D����Ƭ�����ṯ��Һ��ӦAl+Hg2+=Al3++Hg |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��̼����������ϣ�2H++CO32-=CO2��+H2O |
| B��NaHCO3��Һ��NaOH��Һ��Ӧ��HCO3-+OH-=CO2��+H2O |
| C��Al2O3��NaOH��Һ�ķ�Ӧ��Al2O3+2OH-=2AlO2-+H2O |
| D���Ȼ�����Һ�м�������İ�ˮ��Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A���������백ˮ��Ӧ��Al3++3OH-=Al��OH��3�� |
| B�����Ȼ�����ʴӡˢ��·�壺Fe3++Cu=Cu2++Fe2+ |
| C������������Һ����������CO2���壺OH-+CO2=HCO3- |
| D����������ͨ�����������Һ��SO2+ClO-+H2O=SO42-+Cl-+2H+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��ϡ���������Ƭ�ϣ�Fe+3H+�TFe3++H2�� | ||
B��ϡ����������������Һ��ϣ�SO
| ||
| C�����Ȼ�������Һ��ͨ������Fe2++Cl2�TFe3++2Cl- | ||
| D����Ͷ���Ȼ�ͭ��Һ��2Na+Cu2++2H2O�TCu��OH��2+2Na++H2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
| A��2Na+2H2O�T2Na++2OH-+H2�� | ||
B��C
| ||
| C��2Br-+Cl2�T2Cl-+Br2 | ||
| D��OH-+CH3COOH�TCH3COO-+H2O |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com