
| A.强碱性溶液中:Na+、K+、SO42-、AlO2- |
| B.含有0.1 mol·L-1Fe3+的溶液中:K+、Mg2+、Cl-、I- |
| C.无色透明溶液中:HCO3-、Na+、Cl-、OH- |
| D.与铝反应生成H2的溶液中:Na+、Cu2+、Cl-、SO42- |
科目:高中化学 来源:不详 题型:单选题
| A.无色透明的水溶液中:K+、Ba2+、I-、MnO4- |
| B.含有大量NO3-的水溶液中:NH4+、Fe2+、SO42-、H+ |
| C.c(HCO3-)=0.1 mol·L-1的溶液中:Na+、K+、CO32-、Br- |
| D.强碱性溶液中:ClO-、S2-、HSO3-、Na+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=11的溶液中:CO32-、Mg2+、AlO2-、NO3- |
| B.加入Al能放出H2的溶液中:Cl-、HCO3-、SO42-、NH4+ |
| C.由水电离出的c(OH-)=1×10-13 mol·L-1的溶液中:Na+、Ba2+、Cl-、Br- |
| D.有较多Fe3+的溶液中:Na+、NH4+、SCN-、HCO3- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.甲基橙呈红色的溶液:NH4+、Ba2+、AlO2-、Cl- |
| B.遇苯酚显紫色的溶液:I-、K+、SCN-、Mg2+ |
| C.与铝反应产生大量氢气的溶液:NH4+、Na+、CO32-、NO3- |
| D.加入NaOH后加热既有气体放出又有沉淀生成的溶液:Ca2+、HCO3-、NH4+、CH3COO-- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 酸 | 电离平衡常数 |
| 醋酸 | K i=1.75×10-5 |
| 次氯酸 | K i=2.98×10-8 |
| 碳酸 | Ki1=4.30×10-7 Ki2=5.61×10-11 |
| 亚硫酸 | Ki1=1.54×10-2 Ki2=1.02×10-7 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.pH=5的NH4Cl溶液中,由水电离出的c(H+)为10-9 mol/L |
| B.pH=3的醋酸和pH=11的NaOH溶液等体积混合后,pH>7 |
| C.在c(H+):c(OH-)=1:1012的溶液中,Na+、I-、NO3-、SO32-能大量共存 |
| D.0.1 mol/L Na2CO3溶液和0.1 mol/L NaHSO4溶液等体积混合,溶液中c(Na+)+c(H+)=c(CO32-)+c(SO42-)+c(HCO3-)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 HCO3-+H+的平衡常数K1= 。(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1= 。(已知:10-5.60=2.5×10-6)查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在含有0.1mol/LCa2+的溶液中:Na+、K+、ClO-、Cl- |
B.在pH=12的溶液中:NH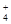 、Na+、SO 、Na+、SO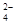 、Cl- 、Cl- |
C.在c(H+)=0.1mol/L的溶液中:K+、I-、Cl-、NO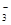 |
D.在澄清透明的无色溶液中:Na+、Cu2+、Cl-、NO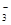 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com