
下列叙述正确的是
A.生成物总能量一定低于反应物总能量
B.酒精可用作燃料,说明酒精燃烧是放热反应
C.硝酸铵溶于水温度降低,这个变化是吸热反应
D.同温同压下,H2和Cl2在光照和点燃条件下的ΔH不同
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
 已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是 ( )
已知C3N4晶体具有比金刚石更大的硬度,且原子间均以单键结合,下列关于C3N4晶体的说法正确的是 ( )
A.C3N4晶体是分子晶体
B.C3N4晶体中微粒间通过离子键结合
C.C3N4晶体中每个C原子连接4个N原子,而每个N原子连接3个C原子
D.C3N4晶体中, C-N键的键长比金刚石中的C-C键的键长要长
查看答案和解析>>
科目:高中化学 来源: 题型:
将标准状况下的aL HCl(g)溶于1000g水中,得到的盐酸密度为b g·cm-3,则该盐酸的物质的量浓度是 ( )
A.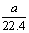 mo1·L-1 B.
mo1·L-1 B.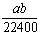 mol·L-1 C.
mol·L-1 C.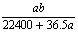 mol·L-1 D.
mol·L-1 D.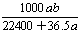 mol·L-1
mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
阿伏加德罗常数的值为6.02×1023mol-1,下列叙述中错误的是:
①12.4g 白磷晶体中含有的P-P键数是0.6×6.02×1023
②含0.2mol H2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0. 1×6.02×1023
③7.8g Na2S和Na2O2的混合物中含有的阴离子数大于0.1×6.02×1023
④2mol SO2和1mol O2在V2O5存在的条件下于密闭容器中加热反应后,容器内物质分子数等于2×6.02×1023
⑤2.9g 2CaSO4•H2O含有的结晶水分子数为0.02×6.02×1023
A.①②③④⑤ B. ①③④⑤ C. ②③④⑤ D. ③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在反应2KMnO4+16HBr===5Br2+2MnBr2+2KBr+8H2O中,还原剂是________。
(2)已知BrFx与H2O按物质的量之比3∶5反应的产物是HF、HBrO3、Br2、O2,该反应中的氧化剂是________,还原剂是________,BrFx中的x=________。
(3)浓盐酸在反应KClO3+HCl―→KCl+ClO2+Cl2+( ) (补充完整此项化学式及化学计量数)中显示出来的性质是_ 。
(4)在一定条件下,PbO2与Cr3+反应,产物是Cr2O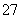 和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为________________。
和Pb2+,则与1 mol Cr3+反应所需PbO2的物质的量为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中充入一定量的N2和O2,在电火花作用下发生反应N2+O2===2NO,经测定前3 s用N2表示的反应速率为0.1 mol·L-1·s-1,则6 s末NO的浓度为
A.1.2 mol·L-1 B.大于1.2 mol·L-1
C.小于1.2 mol·L-1 D.不能确定
查看答案和解析>>
科目:高中化学 来源: 题型:
|
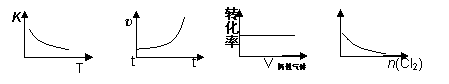
 CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是
CO(g) + Cl2(g) ΔH > 0,当反应达到平衡时,改变一种反应条件,下列示意图正确的是 ① ② ③ ④
A.①表示随温度升高,平衡常数的变化
B.②表示加入催化剂,反应速率随时间的变化
C.③表示恒压条件下,反应物的转化率随充入惰性气体体积的变化
D.④表示CO的体积分数随充入Cl2量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是常见的电化学装置图,①③④中均为惰性电极,下列说法正确的是
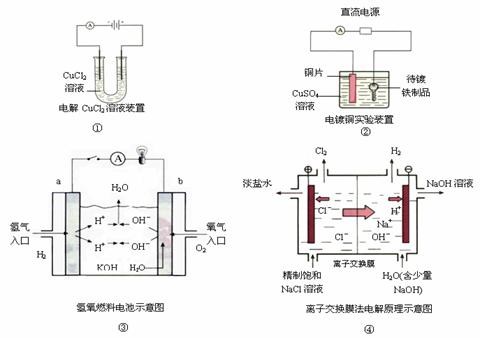
A.装置①中阴极反应式为:2Cl- -2e- = Cl2↑ ,阳极反应式为:Cu2+ + 2e- = Cu
B.装置②中铜片为阳极,若铜片和铁制品的质量相等,电解一段时间后,电路中有2 mol电子转移,此时铜片和铁制品的质量差为128 g
C.装置③中b极为负极,该极的电极反应方程式为O2 + 2H2O + 4e- = 4OH-
D.装置④中阳离子交换膜上每透过1mol Na+时,则阴极上产生11.2L H2
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y为短周期元素,X原子中K、L、M各电子层的电子数之比为1:4:1,Y原子比X原子少3个电子,下列叙述正确的是 ( )北京四中网校
A.X、Y形成化合物表示为X2Y B.X原子半径小于Y的原子半径
C.Y位于周期表中第ⅦA族,其最高正化合价为+7
D.X、Y形成的化合物中所含离子都是10电子微粒
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com