
某探究小组用KMnO4酸性溶液与H2C2O4溶液反应中溶液紫色消失快慢的方法,研究影响反应速率的因素。实验条件作如下限定:所用酸性KMnO4溶液的浓度可选择0.010 mol•L-1、0.0010 mol•L-1, 催化剂的用量可选择0.5 g、0 g,实验温度可选择298 K、323 K。每次实验KMnO4酸性溶液的用量均为4 mL、H2C2O4溶液(0.10 mol•L-1)的用量均为4 mL。
(1)写出反应的离子方程式:
(2)请完成以下实验设计表:完成④的实验条件,并将实验目的补充完整。
实验 编号 | T/K | 催化剂的用量 / g | 酸性KMnO4溶液的浓度/mol•L-1 | 实验目的 |
① | 298 | 0.5 | 0.010 | a. 实验①和②探究酸性KMnO4溶液的浓度对该反应速率的影响; b.实验①和③探究 对反应速率的影响 c. 实验①和④探究催化剂对反应速率的影响。 |
② | 298 | 0.5 | 0.001 | |
③ | 323 | 0.5 | 0.010 | |
④ |
(3)该反应的催化剂选择MnCl2还是MnSO4 ,简述选择的理由 。
(4)某同学对实验①和②分别进行了三次实验,测得以下数据(从混合振荡均匀开始计时):
实验编号 | 溶液褪色所需时间 t / min | ||
第1次 | 第2次[ | 第3次 | |
① | 12.8 | 13.0 | 11.0 |
② | 4.9 | 5.1 | 5.0 |
a、实验②中用KMnO4的浓度变化来表示的平均反应速率为 (忽略混合前后溶液的体积变化)。
b、该同学分析上述数据后得出“当其他条件相同的情况下,酸性KMnO4溶液浓度越小,所需时间就越短,亦即其反应速率越快”的结论,你认为是否正确 (填“是”或“否”)。
C、某同学认为不用经过计算,直接根据褪色时间的长短就可以判断浓度大小与反应速率的关系,你认为应该如何设计实验 。
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案科目:高中化学 来源:2016-2017学年广西柳州铁路一中高二上段考理化学卷(解析版) 题型:选择题
在密闭容器中发生反应mA(g)+nB(g)==pC(g),达到平衡后保持温度不变,将气体体积缩小到原来的1/2,当达到新平衡时,C的浓度为原来的1.9倍,下列说法正确的是( )[来源
A.m+n>p B.平衡向逆反应方向移动
C.A的转化率提高 D.C的体积分数增加
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖南省、醴陵四中高二上期中化学卷(解析版) 题型:选择题
常温下,下列各组离子一定能在指定溶液中大量共存的是( )
A .使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
.使酚酞变红色的溶液中:Na+、Al3+、SO42﹣、Cl﹣
B.水电离的c(H+)=1×10﹣13 mol•L﹣1的溶液中:K+、Na+、AlO2﹣、CO32﹣
C.Kw/c(H+)=1×10﹣13mol•L﹣1的溶液中:NH4+、Ba2+、Cl﹣、NO3﹣
D.与Al反应能放出H2的溶液中:Fe2+、K+、NO3﹣、SO42﹣
查看答案和解析>>
科目:高中化学 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:实验题
“一器多用”可实现多方面的化学实验探究,某课外活动小组学生利用图15所示的仪器组合(省略夹持和净化装置)来完成下列实验,回答下列问题:
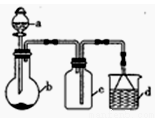
(1)仪器a的名称为______________,仪器a在使用前要________________。
(2)该装置可用于某些气体的制取、收集及尾气处理裝置,下表中3个实验的设计方案合理的是_________________(填序号)
选项 | a中的物质 | b中的物质 | c中收集的气体 | d中的物质 |
A | 稀硝酸 | Cu | NO | H2O |
B | 稀H2SO4 | CaCO3 | CO2 | NaOH溶液 |
C | 浓氨水 | NaOH固体 | NH3 | H2O |
(3)氨气和氯气接触时会产生白烟,请写出相应的化学方程式:_______________________。
(4)上述装置若a中的物质为浓硫酸,b中的物质为Cu片,在加热条件下也可制取SO2。
①下列装置可用于SO2尾气处理的是(夹持仪器已略去)_____________(填序号)。
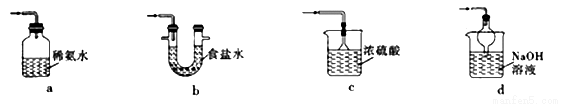
用Fe2(SO4)3溶液也可吸收多余的SO2气体.写出SO2与Fe2(SO4)3溶液反应的离子方程式:_______________________。
②某小组用反应产生的CuSO4溶液来制取胆矾,测定所得胆矾(CuSO4·xH2O)中结晶水x的值,各次 称量的数据如下表:
称量 | 第1次 | 第2次 | 第3次 | 第4次 | 第5次 |
质量(g) | m1=5.4 | m2=8.2 | m3=7.4 | m4=7.2 | m5=7.2 |
则胆矾应放在____________(填仪器名称)中加热;必须要进行恒重操作的原因是__________________;CuSO4·xH2O中的x=___________(保留1位小数);若测定结果x偏大,可能的原因是____________(填序号)。
a.加热温度过高 b.胆矾晶体的颗粒较大 c.加热后放在空气中冷却
查看答案和解析>>
科目:高中化学 来源:2017届云南师大附中高三上月考三化学试卷(解析版) 题型:选择题
化学与社会、生产、生活密切相关,下列说法正确的是
A.氢氧化铝、氢氧化钠都是常见的胃酸中和剂
B.海轮外壳镶嵌锌块是利用牺牲阳极的阴极保护法
C.水泥、玛瑙、分子筛都是硅酸盐工业产品
D.明矾净水时的作用是杀菌、消毒
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三上综合测试三化学卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.高温下,0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3NA
B.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1NA
C.78g苯中含有的碳碳双键数目为3NA
D.1.6 g由氧气和臭氧组成的混合物中含有氧原子的数目 为0.1NA
为0.1NA
查看答案和解析>>
科目:高中化学 来源:2017届陕西西安市高三上模拟三化学试卷(解析版) 题型:实验题
乳酸亚铁([CH3CH(OH)COO]2Fe.3H2O,Mr=288)是一种常用的补铁剂,可通过是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O→[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
已知FeCO3易被氧化:4FeCO3+6H2O+O2=4Fe(OH)3+4CO2。
某兴趣小组用FeCl2(用铁粉和稀盐酸制得)和NH4HCO3制备FeCO3的装置示意图如下:
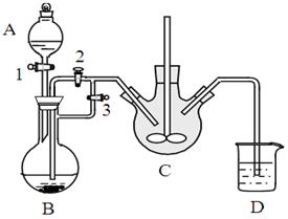
回答下列问题:
(1)NH4HCO3盛放在装置 中(填字母),该装置中涉及的主要反应的离子方程式____________。
(2)将生成的FeCl2溶液和NH4HCO3溶液混合时的操作是_________________。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75℃下搅拌反应。铁粉的作用是________,
反应结束后,无需过滤,除去过量铁粉的方法是 。
(4)该兴趣小组用KMnO4法测定样品中亚铁含量进而计算产品中乳酸亚铁的质量分数,高锰酸钾标准液用_________滴定管盛装(填“酸式”或“碱式”)。下列操作会引起测定结果偏高的是_________。
A.滴定管在盛装高锰酸钾前未润洗
B.滴定过程中,锥形瓶震荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.滴定前读数正确,滴定终点时仰视读数
(5)经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880g产品配成100mL溶液,每次取20.00mL,进行必要处理,用0.1000mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2 19.70mL。滴定反应如下:Ce4++Fe2+=Ce3++Fe3+,则产品中乳酸亚铁的质量分数为 。
查看答案和解析>>
科目:高中化学 来源:2017届陕西省高三上期中化学试卷(解析版) 题型:选择题
下列图示与对应的叙述不相符的是( )
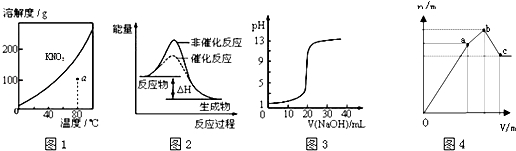
A.图1表示KNO3的溶解度曲线,图中a点所示的溶液是80℃时KNO3的不饱和溶液
B.图2表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化
C.图3表示0.1000mol•L﹣1NaOH溶液滴定20.00mL0.1000mol•L﹣1醋酸溶液得到滴定曲线
D.图4 表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省沭阳县高二上学期期中化学试卷(解析版) 题型:选择题
下列有机物中,不属于卤代烃的是
A.乙苯 B.全氟丙烷 C.氯乙烷 D.氟利昂
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com