
化学与人类生产、生活密切相关,下列有关说法正确的是
A.工业上用惰性电极电解熔融的MgO可制得Mg
B.为加快漂白精的漂白速率,使用时可滴加几滴醋酸
C.草木灰可与铵态氮肥混合施用
D.氢氧化铝、氢氧化钠、碳酸钠都是常见的胃酸中和剂
 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源:2015-2016学年安徽省高二上学期第一次月考化学试卷(解析版) 题型:填空题
已知Fe(s)+CO2(g) 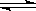 FeO(s)+CO(g) ΔH=a kJ/mol,平衡常数为K;测得在不同温度下,K值如下:
FeO(s)+CO(g) ΔH=a kJ/mol,平衡常数为K;测得在不同温度下,K值如下:
温度/℃ | 500 | 700 | 900 |
K | 1.00 | 1.47 | 2.40 |
(1)该反应的平衡常数表达式K=______________________
(2)方程式中的a________0(填“大于”“小于”或“等于”)。
(3)700℃上述反应达到平衡,要使得该平衡向右移动,其他条件不变时,可以采取的措施有__ ______(填序号)
A.缩小反应器体积 B.通入CO2
C.升高温度到900℃ D.使用合适的催化剂
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江苏省高二上期中选修化学试卷(解析版) 题型:填空题
(10分)NH3经一系列反应可以得到HNO3和NH4NO3,如下图所示。

(1)I中,NH3和O2在催化剂作用下反应,其化学方程式是 。
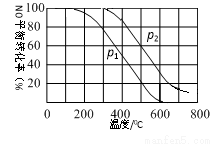
(2)II中,2NO(g)+O2(g)  2NO2(g) 。起始时容器充入1molNO、0.5molO2,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如下图)。
2NO2(g) 。起始时容器充入1molNO、0.5molO2,分别测得NO的平衡转化率在不同压强(p1、p2)下随温度变化的曲线(如下图)。
①比较p1、p2的大小关系 。
②在温度为500℃、压强为p2条件下,平衡混合气中NO2的体积分数 。
(3)III中,将NO2(g)转化成N2O4(l),再制备浓硝酸。
①已知:2NO2(g)  N2O4(g) ΔH1 2NO2(g)
N2O4(g) ΔH1 2NO2(g)  N2O4(l) ΔH2
N2O4(l) ΔH2
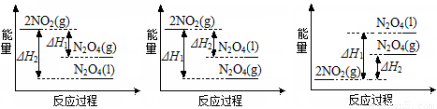
A B C
反应过程中能量变化正确的是 (填序号)。
②N2O4与O2、H2O化合的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期期中测试化学试卷(解析版) 题型:选择题
将一定量的Cl2通入一定浓度的苛性钾溶液中,两者恰好完全反应(已知反应过程放热),生成物中有三种含氯元素的离子,其中ClO-和ClO3-两种离子的物质的量(n)与反应时间(t)的变化示意图如右图所示。下列说法正确的是

A.苛性钾溶液中KOH的物质的量是0.09mol
B.ClO3-的生成是由于氯气的量的多少引起的
C.在酸性条件下ClO-和ClO3-可生成Cl2
D.反应中转移电子的物质的量是0.21mol
查看答案和解析>>
科目:高中化学 来源:2016届河南省林州市高三上学期9月质检化学试卷(解析版) 题型:选择题
已知25℃时:①HF(aq)+OH-(aq) F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
F-(aq)+H2O(l) ΔH=-67.7 kJ/mol
②H+(aq)+OH-(aq)===H2O(l) ΔH=-57.3 kJ/mol下列有关说法中正确的是
A.HF电离:HF(aq) H+(aq)+F-(aq)△H=+10.4KJ/mol
H+(aq)+F-(aq)△H=+10.4KJ/mol
B.水解消耗0.1 mol F-时,吸收的热量为6.77 kJ
C.中和热均为57.3 kJ/mol
D.含0.1 mol HF、0.1 mol NaOH的两种溶液混合后放出的热量为6.77 kJ
查看答案和解析>>
科目:高中化学 来源:2016届吉林省长春市高三上学期质量监测化学试卷(解析版) 题型:选择题
用惰性电极电解NaCl和CuSO4混合液250mL,经过一段时间后,两极均得到11.2 L气体(标准状况),则下列有关描述中,正确的是
A.阳极发生的反应只有:4OH--4e-═2H2O+O2↑
B.两极得到的气体均为混合气体
C.若Cu2+起始浓度为l mol•L-l,则C1-起始浓度为2 mol•L-1
D.Cu2+的起始物质的量应大于0.5 mol
查看答案和解析>>
科目:高中化学 来源:2015-2016学年福建省四地六校高二上学期10月联考化学试卷(解析版) 题型:填空题
(1)根据如图所示情况,判断下列说法中正确的是 。
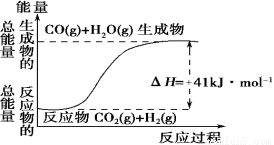
A.其热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g) ΔH=41 kJ·mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.若当H2O为液态时反应热为ΔH2,则ΔH2>ΔH
(2)25℃、101 kPa下,已知1g氢气完全燃烧生成液态水时放出142.9 kJ的热量,该反应的热化学方程式是 。
(3)已知反应: N2(g) + O2 (g) = 2NO(g) △H1
2H2(g) + O2(g) = 2H2O(g) △H2
N2(g) + 3H2(g) = 2NH3(g) △H3
利用上述三个反应,计算4NH3(g) + 5O2(g) = 4NO(g) + 6H2O(g) △H4 的反应焓变为 (用含△H1、△H2、△H3的式子表示)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上学期10月月考化学试卷(解析版) 题型:选择题
在一定条件下,可逆反应X(g)十3Y(g) 2Z(g)达到平衡时,X的转化率与Y的转化率之比为1∶2,则起始充入容器中的X与Y的物质的量之比为
2Z(g)达到平衡时,X的转化率与Y的转化率之比为1∶2,则起始充入容器中的X与Y的物质的量之比为
A.1∶1 B.1∶3 C.2∶3 D.3∶2
查看答案和解析>>
科目:高中化学 来源:2016届江苏省无锡市高三上学期10月月考化学试卷(解析版) 题型:填空题
(15分) 铝铁合金在微电机中有广泛应用,某兴趣小组为利用废弃的铝铁合金设计了如下实验流程制备聚合硫酸铁和明矾:

(1)聚合硫酸铁是一种无毒无害、化学性质稳定、能与水混溶的新型絮凝剂,微溶于乙醇,其化学式可表示为[Fe2(OH)x(SO4)y]n。
①聚合硫酸铁可用于净水的原理是 。
②有人认为上述流程中的“氧化”设计存在缺陷,请提出改进意见: ;浓缩时向其中加入一定量的乙醇,加入乙醇的目的是 。
③加入试剂Y的目的是调节pH,所加试剂Y为 ;溶液的pH对[Fe2(OH) x(SO4)y]n 中x的值有较大影响(如图1所示),试分析pH过小(pH<3)导致聚合硫酸铁中x的值减小的原因: 。

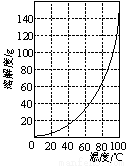
图1 图2
(2)明矾是一种常见铝钾硫酸盐。
①为充分利用原料, 试剂X应为 。
②请结合图2所示的明矾溶解度曲线,补充完整由滤液Ⅰ制备明矾晶体的实验步骤(可选用的试剂:废弃的铝铁合金、稀硫酸、NaOH溶液和酒精):向滤液Ⅰ中加入足量的含铝废铁屑至不再有气泡产生, ,得到明矾晶体。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com