
【题目】实验室通常用MnO2和浓盐酸共热制取Cl2,反应的化学方程式为MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O。
MnCl2+Cl2↑+2H2O。
(1)该反应的氧化剂是_______(填化学名称),氧化产物是_______(填化学式)。
(2)当有73.0克HCl被氧化时,消耗MnO2的物质的量为_______。
(3)当有0.2mol电子转移时,产生氯气的体积(标准状况)是_______L。
【答案】二氧化锰Cl21 mol22.4
【解析】
反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中Mn元素化合价降低,被还原,MnO2为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,Cl2为氧化产物,MnCl2为还原产物,结合电子转移相等解答。
MnCl2+Cl2↑+2H2O中Mn元素化合价降低,被还原,MnO2为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,Cl2为氧化产物,MnCl2为还原产物,结合电子转移相等解答。
(1)反应MnO2+4HCl(浓)![]() MnCl2+Cl2↑+2H2O中Mn元素化合价降低,被还原,二氧化锰为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,Cl2为氧化产物,MnCl2为还原产物;
MnCl2+Cl2↑+2H2O中Mn元素化合价降低,被还原,二氧化锰为氧化剂,Cl元素化合价升高,被氧化,HCl为还原剂,Cl2为氧化产物,MnCl2为还原产物;
(2)73.0g氯化氢的物质的量是n(HCl)=73g÷36.5g/mol=2mol,1分子氯化氢被氧化失去1个电子,则转移2mol电子。Mn元素化合价从+4价降低到+2价,得到2个电子,根据电子得失守恒可知消耗MnO2的物质的量为2mol÷2=1mol;
(3)根据以上分析可知每生成1分子氯气,转移2个电子,则当有0.2mol电子转移时,产生氯气的物质的量是0.2mol÷2=0.1mol,在标况下的体积为0.1mol×22.4L/mol=2.24L。


 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是

A. 放电时,右槽发生还原反应
B. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
C. 充电时,每转移1mol电子,n(H+)的变化量为1mol
D. 充电时,阴极电解液pH升高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国化学家合成了一种新型除草剂的合成路线如下:

(1)① 中两种含氧官能团的名称_______、_____。除草剂⑦的分子式为_______ 。
(2)③与⑥生成⑦的反应类型是____,④⑤转化中另外一种产物是HCl,则试剂X是_____ 。
(3)写出一种同时满足下列条件的物质③的同分异构体的结构简式______________。
① 属于芳香族化合物; ② 苯环上的一取代物只有两种;
③ 在铜催化下与O2反应,其生成物1 mol与足量的银氨溶液反应生成4 mol Ag
(4)写出②③的化学方程式__________________________________________。
(5)卡巴拉丁是老年人认知障碍的重要治疗药物。请结合上述合成路线及下面所给的反应:![]()
ROH+SOCl2RCl+HOSOCl
请写出合成卡巴拉丁流程中A、B、D的结构简式,C试剂的化学式。

A:____________、B:_____________、C:____________、D:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列常见的化合物的溶液中滴入足量氨水,最后不生成沉淀的是( )
A. AlCl3溶液
B. FeCl3溶液
C. MgSO4溶液
D. CuSO4溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有A、B、C、D、E、F六种装置,如图所示。(胶塞、导管可自由选用)


(1)写出①~④的仪器名称:①__________,②__________,③________,④________。
(2)实验室制取并收集氧气时应选择________和________相连接,制取并收集氢气时应选择________和________相连接。
(3)做木炭还原氧化铜并检验生成气体的实验,应选择________和________相连接,检验气体时观察到的实验现象是__________________________________________________。
(4)制取氢气并做还原氧化铜的实验,应选择________和________装置,实验结束时应先停止加热,待试管冷却后,再停止通氢气,其原因是______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ /mol;HCl(aq)与NaOH(aq)反应的△H =-55.6kJ/ mol。则HCN在水溶液中电离的ΔH等于
A. -67.7 kJ /mol B. -43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)2molO3和3molO2的质量之比为________,分子数之比为________,同温同压下的密度之比为________。
(2)在标准状况下,由CO和CO2组成的混合气体6.72L,质量为12g,此混合物中CO和CO2物质的量之比是____,混合气体的平均相对分子质量是_____,对氢气的相对密度是____。
(3)19 gACl2中含有0.4 mol Cl-,则该氯化物的摩尔质量是_____;A的相对原子质量是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某碱性蓄电池在充电和放电时发生的反应为:Fe+NiO2+2H2O![]() Fe(OH)2+Ni(OH)2,下列说法中正确的是
Fe(OH)2+Ni(OH)2,下列说法中正确的是
A. 充电时,阳极附近pH值减小
B. 充电时,阴极反应是:Ni(OH)2-2e-+2OH-=NiO2+2H2O
C. 放电时,负极上发生反应的物质是Fe(OH)2
D. 放电时,正极反应是:NiO2+2e-+2H+=Ni(OH)2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】侯德榜是在中国化学工业史上一位杰出的科学家,他为祖国的化学工业事业奋斗终生,并以独创的制碱工艺闻名于世界,以下是侯德榜先生制碱工业的简要流程:
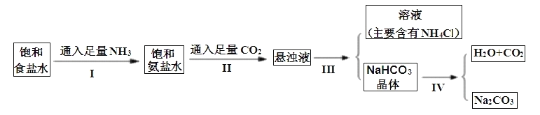
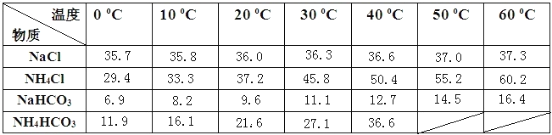
下表是四种物质在100g水中不同温度的溶解度,其中NH4HCO3水溶液呈碱性,性质不稳定,36℃时开始分解为二氧化碳、氨和水,60℃可以分解完。
试回答下列问题:
(1)IV的反应条件是加热,请尝试写出IV的反应方程式:________________________。
(2)Ⅲ的操作名称叫____________。
(3)通过上述溶解度表,如何从含有少量NaCl的NH4Cl溶液中获得NH4Cl晶体:_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com