
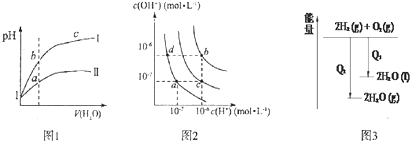
| A. | 图l表示同温度下,pH=1的盐酸和醋酸溶液分别加水稀释时pH的变化曲线,其中曲线Ⅱ为盐酸,且b点溶液的导电性比a点强 | |
| B. | 图2中纯水仅升高温度,就可以从a点变到c点 | |
| C. | 图2中在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显中性 | |
| D. | 图3表示氢气与氧气反应中的能量变化 |
分析 A.醋酸为弱酸,稀释促进电离,加水稀释后醋酸pH较小;
B.纯水仅升高温度,氢离子和氢氧根离子浓度均增大;
C.b点Kw=10-12,中性溶液pH=6;
D.H2(g)与O2(g)反应生成H2O(l)或H2O(g)为放热反应.
解答 解:A.醋酸为弱酸,稀释促进电离,加水稀释后醋酸pH较小,曲线Ⅱ为醋酸,且b点溶液的导电性比a点弱,故A错误;
B.纯水仅升高温度,氢离子和氢氧根离子浓度均增大,图2中从a点变到c点,氢氧根离子浓度不变,故B错误;
C.b点Kw=10-12,中性溶液PH=6;将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,氢离子浓度和氢氧根离子浓度相同,等体积混合溶液呈中性,故C正确;
D.H2(g)与O2(g)反应生成H2O(l)或H2O(g)为放热反应,气体水变化为液体水放热,图象能量大小关系错误,故D错误.
故选C.
点评 本题以图象的形式弱电解质的电离、pH的有关计算、能量变化图等,题目难度中等,需要学生具有扎实的基础知识与读图获取信息的能力.


科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
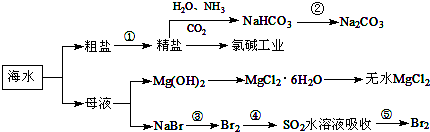
| A. | 要实现反应②可向NaHCO3溶液中加入过量石灰水 | |
| B. | 氯碱工业中采用阴离子交换膜提高产品纯度 | |
| C. | MgCl2溶液加热蒸干可得无水MgCl2 | |
| D. | 溴元素在反应③、⑤中均被氧化,在反应④中被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 编号 | NaOH/mol•L-1 | HA/mol•L-1 | 混合溶液的pH |
| ① | 0.1 | 0.1 | pH=9 |
| ② | c | 0.2 | pH=7 |
| ③ | 0.1 | 0.2 | pH<7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
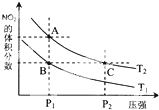 氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是
氮可形成多种氧化物,如NO、NO2、N2O4等.已知NO2和N2O4的结构式分别是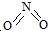 和
和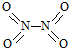 .实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.
.实验测得N-N键键能为167kJ•mol-1,NO2中氮氧键的平均键能为466kJ•mol-1,N2O4中氮氧键的平均键能为438.5kJ•mol-1.| 时间(s) | 0 | 20 | 40 | 60 | 80 |
| n(NO2)/mol | 0.40 | n1 | 0.26 | n3 | n4 |
| n(N2O4)/mol | 0.00 | 0.050 | n2 | 0.080 | 0.080 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要用到的玻璃仪器有玻璃棒、烧杯、量筒、胶头滴管和容量瓶 | |
| B. | 量取浓硫酸的体积为24 mL | |
| C. | 将蒸馏水缓慢注入盛有一定量浓硫酸的烧杯中,不断搅拌并冷却至室温 | |
| D. | 先在容量瓶中加入适量水,将量好的浓硫酸注入容量瓶,加水定容 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 44 g CO2的体积是22.4 L | |
| B. | NH3的摩尔质量是17g/mol | |
| C. | 100 mL 1 mol/L NaCl溶液中含有1 mol Cl- | |
| D. | 标准状况下,11.2 L H2O中含有3.01×1023个水分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )
莽草酸是一种合成治疗禽流感药物达菲的原料,鞣酸存在于苹果、生石榴等植物中.有关说法正确的是( )| A. | 等浓度的两种酸其酸性相同 | |
| B. | 两种酸都能与溴水发生加成反应 | |
| C. | 鞣酸分子与莽草酸分子相比多了两个碳碳双键 | |
| D. | 鞣酸能与Fe3+发生显色反应,而莽草酸不能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com