
����Ŀ���������ֿ��������ʼס��ҡ����������죬�������������������ӻ�����ͬ���ֱ�������������K+��Al3+��Cu2+��Ba2+��Fe3+������������Cl����OH����NO ![]() ��CO
��CO ![]() ��X�е�һ�֣�
��X�е�һ�֣�
��1��ijͬѧͨ�������Ƚϣ���Ϊ�������Ϳ��ж����б��е������������� �� ���ѧʽ��
��2�����ʱ��к�������X��Ϊ��ȷ��X���ֽ���1���е��������ʼ�Ϊ���ң����������Һ���ʱ������ɫ��������ó����е�������ϡ���ᣬ���������ܽ⣬ʣ���ɫ���壬�����ʱ�Ϊ �� ���ѧʽ��
��3����19.2g CuͶ��װ����������Һ���Թ��У�Cu���ܽ⣬�ٵμ�ϡ���ᣬCu���ܽ⣬�ܿڸ����к���ɫ������֣�д��Cu�ܽ�����ӷ���ʽ �� ��Ҫ��Cu��ȫ�ܽ⣬���ټ�����������ʵ����� ��
��4������Һ������ᷴӦʱ��������ɫ���ʣ��÷�Ӧ�����ӷ���ʽΪ ��
���𰸡�
��1��K2CO3��Ba��OH��2
��2��CuSO4
��3��3Cu+8H++2NO3���T3Cu2++2NO��+4H2O��0.4mo
��4��2Fe3++2I��=2Fe2++I2
���������⣺CO ![]() ��Fe3+��Cu2+��Ba2+��Al3+���ܴ������棬OH����Fe3+��Cu2+��Al3+���ܴ������棬����е��������ʼ�Ϊ�ס��ң��ס��ҷֱ�ΪK2CO3��Ba��OH��2 �� �������Һ���ʱ������ɫ��������ó����е�������ϡHNO3 �� ���������ܽ⣬ʣ���ɫ���壬��ɫ����Ϊ������ͭ����ɫ����Ϊ���ᱵ�����ӦΪBa��OH��2 �� ���к�SO
��Fe3+��Cu2+��Ba2+��Al3+���ܴ������棬OH����Fe3+��Cu2+��Al3+���ܴ������棬����е��������ʼ�Ϊ�ס��ң��ס��ҷֱ�ΪK2CO3��Ba��OH��2 �� �������Һ���ʱ������ɫ��������ó����е�������ϡHNO3 �� ���������ܽ⣬ʣ���ɫ���壬��ɫ����Ϊ������ͭ����ɫ����Ϊ���ᱵ�����ӦΪBa��OH��2 �� ���к�SO ![]() �����ΪCuSO4 �� ��CuͶ��װ����������Һ���Թ��У�Cu���ܽ⣬�ٵμ�ϡ���ᣬCu���ܽ⣬�ܿڸ����к���ɫ������֣�����Һ������ᷴӦʱ��������ɫ���ʣ���ΪAl��NO3��3 �� ��ΪFeCl3 �� ��1��������������֪�����е���������ΪK2CO3��Ba��OH��2 �� ���Դ��ǣ�K2CO3��Ba��OH��2����2���������Һ���ʱ������ɫ������˵�����к�Cu2+ �� ������ϡ������������ܽ⣬˵�����к�Ba��OH��2 �� ���к�SO42�� �� ����ΪCuSO4 �� ���Դ��ǣ�CuSO4����3������ɫ���壬ΪNO������е�������Ӧ���ɵ�NO2 �� ���к���NO
�����ΪCuSO4 �� ��CuͶ��װ����������Һ���Թ��У�Cu���ܽ⣬�ٵμ�ϡ���ᣬCu���ܽ⣬�ܿڸ����к���ɫ������֣�����Һ������ᷴӦʱ��������ɫ���ʣ���ΪAl��NO3��3 �� ��ΪFeCl3 �� ��1��������������֪�����е���������ΪK2CO3��Ba��OH��2 �� ���Դ��ǣ�K2CO3��Ba��OH��2����2���������Һ���ʱ������ɫ������˵�����к�Cu2+ �� ������ϡ������������ܽ⣬˵�����к�Ba��OH��2 �� ���к�SO42�� �� ����ΪCuSO4 �� ���Դ��ǣ�CuSO4����3������ɫ���壬ΪNO������е�������Ӧ���ɵ�NO2 �� ���к���NO ![]() ����֪��19.2gCuͶ��װ������D��Һ���Թ��У�Cu���ܽ⣻�ٵμ�ϡH2SO4 �� Cu���ܽ⣬ �����ķ�ӦΪ3Cu+8H++2NO
����֪��19.2gCuͶ��װ������D��Һ���Թ��У�Cu���ܽ⣻�ٵμ�ϡH2SO4 �� Cu���ܽ⣬ �����ķ�ӦΪ3Cu+8H++2NO ![]() �T3Cu2++2NO��+4H2O��
�T3Cu2++2NO��+4H2O��
��n��Cu��= ![]() =0.3mol��
=0.3mol��
�ɷ��̿�֪ ![]() =
= ![]() ��
��
����n��H+��=0.8mol��
����n��H2SO4��=12n��H+��=0.4mol��
���Դ��ǣ�3Cu+8H++2NO ![]() �T3Cu2++2NO��+4H2O��0.4mol����4�����м�����ᣬ������ɫ����ΪI2 �� ˵�����к����������ӣ�ֻ����Fe3+ �� ���ӷ�ӦΪ2Fe3++2I��=2Fe2++I2 �� ���Դ��ǣ�2Fe3++2I��=2Fe2++I2 ��
�T3Cu2++2NO��+4H2O��0.4mol����4�����м�����ᣬ������ɫ����ΪI2 �� ˵�����к����������ӣ�ֻ����Fe3+ �� ���ӷ�ӦΪ2Fe3++2I��=2Fe2++I2 �� ���Դ��ǣ�2Fe3++2I��=2Fe2++I2 ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧʵ������У�����ȷ���ǣ�������
A. �õ�ñ����ƾ��ƵĻ���
B. ϡ��Ũ����ʱ����Ũ���Ỻ���ӵ�ˮ�У��������ò���������
C. ��������������ֱ�ӷ���������ƽ�ϳ���
D. ���Թ���Ĺ�����ȣ��Թܿ�Ӧ����������б
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����50mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ����к��ȣ��ش��������⣺ 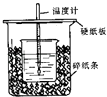
��1����ʵ��װ���Ͽ���ͼ����ȱ�ٵ�һ�ֲ�����Ʒ�� ��
��2���ձ���������ֽ���������� ��
��3�����ձ����粻��Ӳֽ�壬��õ��к�����ֵ���ƫ��ƫС����Ӱ�족��
��4�������60mL 0.50mol/L������50mL 0.55mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų������������ȡ�����ȡ����������к��������ȡ�����ȡ�������������
��5������ͬŨ�Ⱥ�����İ�ˮ��NH3H2O������NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ�������ƫ����ƫС��������Ӱ�족����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ⱦɫ����ͷ�������и���Ǧ(PbCrO4)����ɫΪ���ʻƣ���ʹ�����°����ѱ����������Ľ��á���֪��Ԫ�أ�Cr�����ϼ�Ϊ+6�ۣ���ǦԪ�صĻ��ϼ�Ϊ�� ��
A. +2B. +4C. +5D. +7
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ʳ��ڱ�¶�ڿ����л���ʣ�ͬʱ�������ӵ���
A. ����ʯ B. ������ C. Ũ���� D. �Ȼ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ԫ��W��X��Y��Z ��ԭ��������������W��Y��X��Z λ��ͬһ���壮W��X���γɹ��ۻ�����WX2 �� Yԭ�ӵ��ڲ������������������������2.5 �����������в���ȷ���ǣ� ��
A.WX2����������ԭ������㶼Ϊ8���ӽṹ
B.WX2��ZX2�Ļ�ѧ�����ͺ;������Ͷ���ͬ
C.WX2���Լ��Լ���ϳɵķǼ��Է���
D.ԭ�Ӱ뾶��С˳��ΪX��W��Y��Z
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A. 1 mol��Ϊ2 g B. H2O��Ħ������Ϊ18 g
C. 44 g CO2�����Ϊ22.4 L D. 9.8 g H2SO4��0.1NA��H2SO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ԫ��X λ�ڵ������ڣ����̬ԭ�ӵ��ڲ���ȫ���������ӣ�������������Ϊ2��Ԫ��Y��̬ԭ�ӵ�3p�������4�����ӣ�Ԫ��Z��ԭ�����������������ڲ��3����
��1����Y���⻯�H2Y�������У�Yԭ�ӹ�����ӻ������� ��
��2��Z���⻯�H2Z�����Ҵ��е��ܽ�ȴ���H2Y����ԭ���� ��
��3��Y��Z���γ�YZ42��
��YZ42���Ŀռ乹��Ϊ����������������
��д��һ����YZ42����Ϊ�ȵ�����ķ��ӵĻ�ѧʽ�� ��
��4��X���Ȼ����백ˮ��Ӧ���γ������[X��NH3��4]Cl2 �� 1mol��������к��ЦҼ�����ĿΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӷ���ʽ�У���ȷ���ǣ� ��
A.����ͨ������У�CH3COOH+NH3�TCH3COO��+NH![]()
B.��̼����þ��Һ�мӹ���ʯ��ˮ��Mg2++2HCO ![]() +Ca2++2OH���TCaCO3��+2H2O+MgCO3��
+Ca2++2OH���TCaCO3��+2H2O+MgCO3��
C.����ʯ��ˮ��ϡ���ᷴӦ��Ca��OH��2+2H+�TCa2++2H2O
D.ϡ�������ͭƬ�ϣ�Cu+2H+�TCu2++H2��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com