
| A、铁和氯气反应生成三价铁,和盐酸反应生成亚铁离子 |
| B、铜在潮湿的空气中易生锈呈绿色,锈的主要成分是碱式碳酸铜 |
| C、过氧化钠和氧化钠均可以与水、二氧化碳反应,但生成的产物不完全相同 |
| D、等质量的铝分别与足量的酸和碱溶液反应,生成气体的体积一定相同 |


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
| A、③④ | B、③ | C、②③ | D、①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、全部 | B、①②⑤⑥ |
| C、②⑤ | D、①⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、钠与氧气在常温下反应生成氧化钠 |
| B、将钠置于干燥的氧气中充分反应,可能有过氧化钠生成 |
| C、钠易与氧气反应,但不能跟其他非金属反应 |
| D、将钠置于空气中一段时间,可能有碳酸钠生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2S、NH3、SO3 |
| B、CO2、NH4Cl、Na2O2 |
| C、N2、CS2、NO |
| D、CaO、H2O2、CH4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正反应方向移动了 |
| B、平衡向逆反应方向移动了 |
| C、物质B的质量分数减小了 |
| D、a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清石灰水、浓硫酸 |
| B、KMnO4酸性溶液、浓硫酸 |
| C、溴水、浓硫酸 |
| D、浓硫酸、KMnO4酸性溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
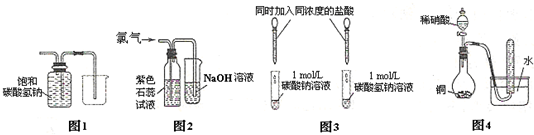
| A、①② | B、②④ | C、①④ | D、②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:
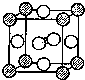 X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素.
X、Y、D、E、M、N是原子序数依次增大的前四周期元素,其中X是周期表中原子半径最小的元素,Y元素基态原子的三个能级上电子数目相同,E是地壳中含量最多的元素,M是制常见不锈钢材料的第一主要合金元素,其基态原子核外的未成对电子数在同周期元素中最多,N是目前用量最大的金属元素. 表示,镍原子用
表示,镍原子用 表示,镁原子用
表示,镁原子用 表示),则该晶体的化学式:
表示),则该晶体的化学式:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com