
| A.饱和石灰水跟稀硝酸反应Ca(OH)2 + 2H+ = Ca2+ + 2H2O |
| B.钠和水反应Na+2H2O=Na++H2↑+2OH- |
| C.大理石与盐酸反应 CaCO3+2H+=Ca2++H2O+CO2↑ |
| D.硫酸与氢氧化钡溶液反应 Ba2++OH-+H++SO42-= BaSO4↓+ H2O |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.H+、Ba2+、HCO3-、Cl- | B.K+、Fe3+、I-、NO3- |
| C.NH4+、AlO2-、Cl-、OH- | D.K+、SO42-、S2-、Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
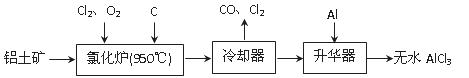
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.K+一定存在 |
| B.100 mL溶液中含0.01 mol CO32— |
| C.Cl-可能存在 |
| D.Ba2+一定不存在,Mg2+可能存在 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 步骤 | 操作 | 现象 |
| (1) | 用pH试纸检验 | 溶液的pH大于7 |
| (2) | 向溶液中滴加氯水,再加入CCl4振荡,静置 | CCl4层呈橙色 |
| (3) | 向所得水溶液中加入Ba(NO3)2溶液和稀硝酸 | 有白色沉淀产生 |
| (4) | 过滤,向滤液中加入AgNO3溶液和稀硝酸 | 有白色沉淀产生 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.NH4+ NO3- CO32- Na+ |
| B.Na+Ba2+Mg2+HCO3- |
| C.NO3- K+AlO2- OH- |
| D.NO3- Ca2+K+Cl- |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
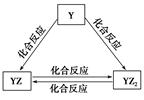
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com