
【题目】下列物质属于单质的是
A. 石墨 B. 硫铁矿 C. 青铜 D. 碳素墨水
科目:高中化学 来源: 题型:
【题目】掌握仪器名称、组装及使用方法是中学化学实验的基础,如图为实验装置. 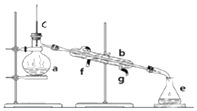
(1)写出下列仪器的名称:
a.b.c.
(2)利用装置分离四氯化碳和酒精的混合物,还缺少的仪器是 , 将仪器补充完整后进行实验,温度计水银球的位置在处.
(3)冷凝水由(填f或g)口通入.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学实验小组为验证常见还原剂SO2、I-、Fe2+的还原性强弱的顺序为:SO2>I->Fe2+,用下图所示装置进行实验(加热和夹持装置已略,气密性已检验)。

(1)上述实验需要加热的装置是__________
(2)A中反应的化学方程式为________,
(3)D中,烧杯盛放的是_______
(4)实验开始时,关闭K1,打开K2,通入少量氯气,写出B中发生反应的离子方程式____________
①为验证I-的还原性比Fe2+强,取(4)后B中的少量溶液于试管中,应再往试管中滴入______溶液,现象是______
②在(4)后,为了比较SO2和I-的还原性强弱,接下来的操作是____
A.打开K1 B.打开K2 C.同时打开K1和K2
(5)若打开K2,通入Cl2恰好将Fe2+、I-全部氧化后,再打开K1通入SO2,当Fe3+全部转化为Fe2+时,此时通入的SO2的体积(标准状况下)为_______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的分类组合正确的是
A | B | C | D | |
纯净物 | 空气 | NaOH | 稀盐酸 | FeSO4·7H2O |
非电解质 | H2O | Na2O | CO | NH3 |
电解质 | HNO3 | Cu | 蔗糖 | CH3COOH |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用氧化铝作原料,碳热法冶铝的两步反应为:
①2173~2473K时:2Al2O3+9C![]() Al4C3+6CO↑;
Al4C3+6CO↑;
②温度高于2473K时:Al2O3+Al4C3![]() 6Al+3CO↑.
6Al+3CO↑.
下列有关说法不正确的是( )
A. A12O3属于两性氧化物
B. 两步反应中CO均是氧化产物
C. Al4C3与盐酸反应可生成烃,该烃为乙烯
D. 生成的铝粉不能在空气中冷却
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某无色废水中可能含有H+、NH4+、Fe3+、Al3+、Mg2+、Na+、NO3-、CO32-、SO42-中的几种,为分析其成分,分别取废水样品100 mL,进行了三组实验,其操作和有关图像如下所示:


请回答下列问题:
(1)根据上述3组实验可以分析废水中一定不存在的离子有____________________。
(2)实验③中所发生反应的离子反应方程式为___________________________。
(3)依据图2判断出的原溶液中阳离子的种类及物质的量的比值为________。
(4)原溶液中NO3-是否存在?________ (“存在”、“不存在”或“不确定”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2A(g)+B(g)3C(g)+4D(g)的反应,在不同条件下的反应的速率最快的是( )
A.v(A)=0.7 mol/(L.min)
B.v(B)=0.3mol/(L.min)
C.v(C)=0.9 mol/(L.min)
D.v(D)=1.1mol/(L.min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx . 已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=﹣574kJmol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=﹣1160kJmol﹣1
则甲烷直接将NO2还原为N2的热化学方程式为 .
(2)利用反应6NO2+8NH3 ![]() 7N2+12H2O处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
7N2+12H2O处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g);△H<0.该反应的化学平衡常数表达式为K= , 该反应△S0(填“>”或“<”)若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将移动(填“向左”、“向右”或“不”).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是(填序号).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42﹣而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4).已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com