
分析 (1)根据常见材料的性能和用途进行分析;
(2)可降解塑料是指在生产过程中加入一定量的添加剂(如淀粉、改性淀粉或其它纤维素、光敏剂、生物降解剂等),稳定性下降,较容易在自然环境中通过光或微生物降解的塑料;
(3)根据铁制品生锈的条件,铁制品与氧气和水隔绝就可以防止钢铁生锈,也可改变金属内部结构、电化学防护等,据此进行分析解答;
(4)处理污水的化学方法有:混凝法、中和法、沉淀法,根据相应的污水处理原理分析;
(5)室内空气的污染有时比室外更严重.室内空气污染的来源厨房燃烧产生的油烟、建筑装潢材料散发的有机物.
解答 解:(1)透气性陶瓷为硅酸盐产品,由黏土高温烧制而成,具有耐高温和绝缘性,光导纤维主要成分为二氧化硅,具有良好的导光性,水泥是传统的硅酸盐产品,常用于建筑材料,具有水硬性,不锈钢为合金,具有强抗腐蚀性,橡胶具有良好的弹性,天然纤维,具有良好的透气性,如棉花等,
故答案为:③;②;①;⑤;④;⑥;
(2)白色污染是人们对难降解的塑料垃圾(多指塑料袋)污染环境现象的一种形象称谓,使用一些新型的可降解塑料,如生物降解塑料和光降解塑料等,可防止“白色污染”,
故答案为:光降解;微生物;
(3)防止铁制品生锈,除了保持铁制品干燥外,还有很多其它方法,如隔绝氧气可以防止铁生锈,在铁制品表面涂油漆(表面保护膜法)、镀一层金属等方法可以使铁制品与氧气隔绝,也可形成合金(改变内部结构),在潮湿的环境中,铁、碳和电解质溶液构成原电池而产生电流,所以可采用电化学防护(牺牲活泼金属),
故答案为:表面保护膜法;形成合金(改变内部结构);电化学防护(牺牲活泼金属);
(4)处理污水的化学方法有:混凝法是向污水中加入混凝剂,使细小的悬浮颗粒聚集成较大的颗粒而沉淀,与水分离,从而除去水中的悬浮物;中和法是让显酸性的物质能和显碱性的物质发生中和反应;化学沉淀法是向污水中加入特殊的化学物质可以使污水中的污染物以沉淀的形式从水中析出的方法,
故答案为:混凝法、中和法、沉淀法;
(5)室内空气的污染有时比室外更严重.室内空气污染的来源:厨房燃料燃烧产生气体和烹调产生油烟;家具、墙纸、化纤地毯、塑料地毯等会不同程度地释放出某种有害气体甲醛,所以建筑材料和装饰材料挥发的有机物,
故答案为:厨房燃料燃烧产生气体和烹调产生油烟;建筑材料和装饰材料挥发的有机物.
点评 本题考查有关材料的化学,涉及材料的性能、白色污染、金属防锈、污水处理、室内空气污染等知识,侧重于化学与生活的考查,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 实验现象 | 结 论 |
| A | 在平衡3KSCN+FeCl3?Fe(SCN)3+3KCl的溶液中加入少量 KCl溶液 | 溶液红色变浅 | 增大c(KCl),平衡逆向移动 |
| B | 分别向盛有直馏汽油和裂化汽油的试管中加入几滴溴水 | 直馏汽油中溴水褪色,裂化汽油中溴水不褪色. | 可以用溴水鉴别直馏汽油和裂化汽油 |
| C | 向某卤代烃中加入稀NaOH溶液共煮几分钟,然后加入足量稀硝酸,再加入AgNO3溶液 | 产生黄色沉淀 | 该卤代烃中含碘原子 |
| D | 向油脂皂化反应后的溶液中滴入酚酞 | 溶液变红 | 油脂已经完全皂化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
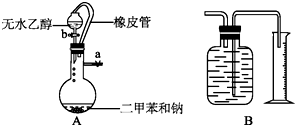 为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.
为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
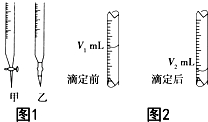 现用物质的量浓度为a mol•L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:
现用物质的量浓度为a mol•L-1的标准NaOH溶液去滴定V mL盐酸的物质的量浓度,请填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH>7,且c(Na +)>c(OH -)>c(H +)>c(CH3COO-) | |
| B. | pH>7,且c(Na +)+c(H+)=c(CH3COO -)+c(OH-) | |
| C. | PH<7,且c(CH3COO -)>c(H+)>c(Na+)>c(OH-) | |
| D. | pH=7,且c(CH3COO -)=c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
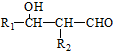
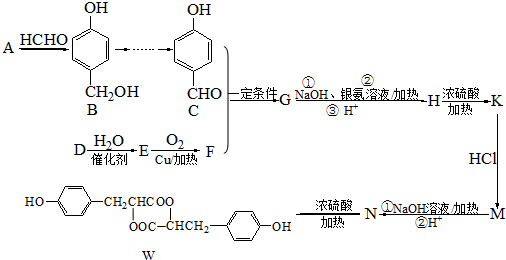
 .
.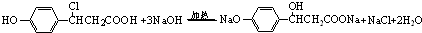 .
.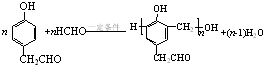 .
.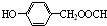 .
.查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第一次月考化学卷(解析版) 题型:推断题
现有三种可溶物质A、B、C,其中A、B是盐,一种是酸式盐,一种是正盐,C是碱,它们溶于水后电离产生的所用离子如下表所示:
阳离子 |
|
阴离子 |
|
请根据下列叙述回答问题:
(1)C的化学式为_________________。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为_______________________, 该反应的离子方程式为___________________.
该反应的离子方程式为___________________.
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为____________,鉴别溶液中B的阴离子的方法是____________________.
②D溶于稀硝酸的离子方程式为________________________.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com