
【题目】X、Y、Z、W、R、Q是原子序数依次增大的前20号元素。X2是通常状况下密度最小的气体;Z与R同主族,R的一种固体单质在空气中易自燃;Y、W最外层电子数之和是Z的2倍,W有W2、W3两种常见单质;含Q的化合物焰色反应呈紫色。请回答下列问题:
(1)X、W、R、Q原子半径由大到小的顺序是(写元素符号)__________;请写出Z在周期表中的位置____________________。
(2)由上述元素组成的物质YW(ZX2)2是一种中性肥料,请写出它的电子式______________。
(3)请设计实验比较Z与R元素的非金属性强弱____________________。
(4)X、Y形成的化合物中含有非极性键且相对分子质量最小的物质是________。(写化学式)
(5)R的简单氢化物具有强还原性,将其通入硫酸铜溶液能生成两种最高价含氧酸和一种单质,请写出该反应的化学方程式__________________________________________________。
(6)Y的最高价氧化物与Q的最高价氧化物的水化物按物质的量之比1:2反应,所得溶液中离子浓度由大到小的顺序____________________。
【答案】K>P>O>H 第二周期ⅤA族 ![]() 配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N C2H2 4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4 c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N C2H2 4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4 c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)
【解析】
X、Y、Z、W、R、Q是原子序数依次增大的前20号元素;X2是通常状况下密度最小的气体,说明X为H元素;Z与R同主族,R的一种固体单质在空气中易自燃,此单质为P4,则Z为N元素,R为P元素;Y、W最外层电子数之和是Z的2倍,W有W2、W3两种常见单质,则W为O元素,Y为C元素;含Q的化合物焰色反应呈紫色,可知Q为K元素,据此分析并结合元素周期律分析解题。
由分析知:X、Y、Z、W、R、Q依次为H、C、N、O、P、K元素;
(1)H、O、P、K原子分属四个不同周期,结合同主族元素核电荷数大,原子半径大,而同周期主族元素,核电荷数大,原子半径小的规律可知原子半径K>Na>P>S>O>H,则半径由大到小的顺序是(写元素符号) K>P>O>H;Z为N元素,核电荷数为7,其在周期表中的位置第二周期ⅤA族;
(2)由上述元素组成的尿素(CO(NH2)2是一种中性肥料,说明其为共价化合物,则它的电子式为![]() ;
;
(3)元素的非金属性越强,其最高价氧化物水化物的酸性越强,则配制等浓度的磷酸和硝酸溶液,分别测量其pH,磷酸溶液的pH大,说明硝酸的酸性强,即P的非金属性弱于N;
(4)C、H元素可组成多种烃,其中含有非极性键且相对分子质量最小的物质是乙炔,其化学式为C2H2;
(5)PH3具有强还原性,通入硫酸铜溶液能生成两种最高价含氧酸和一种单质,应为磷酸、硫酸和Cu,则发生反应的化学方程式为4CuSO4+PH3+4H2O=4Cu↓+H3PO4+4H2SO4;
(6)CO2与KOH按物质的量之比1:2反应生成K2CO3,所得溶液中CO32-分步水解,且溶液呈碱性,则溶液中离子浓度由大到小的顺序为c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+)。


科目:高中化学 来源: 题型:
【题目】化学一选修:化学与技术磷矿石主要以[Ca3(PO4)2H2O]和磷灰石[Ca5F(PO4)3,Ca5(OH)(PO4)3]等形式存在,图(a)为目前国际上磷矿石利用的大致情况,其中湿法磷酸是指磷矿石用过量硫酸分解制备磷酸,图(b)是热法磷酸生产过程中由磷灰石制单质磷的流程:
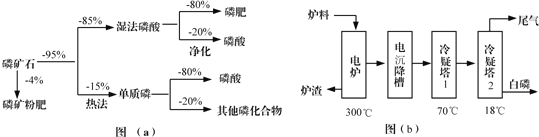
部分物质的相关性质如下:
熔点/℃ | 沸点/℃ | 备注 | |
白磷 | 44 | 280.5 | |
PH3 | -133.8 | -87.8 | 难溶于水、有还原性 |
SiF4 | -90 | -86 | 易水解 |
回答下列问题:
(1)世界上磷矿石最主要的用途是生产含磷肥料,约占磷矿石使用量的____________;
(2)以磷矿石为原料,湿法磷酸过程中Ca5F(PO4)3反应的化学方程式为:___________,现有1t折合含有P2O5约30%的磷灰石,最多可制得到85%的商品磷酸___________t。
(3)如图(b)所示,热法磷酸生产过程的第一步是将SiO2、过量焦炭与磷灰石混合,高温反应生成白磷,炉渣的主要成分是___________(填化学式),冷凝塔1的主要沉积物是___________,冷凝塔2的主要沉积物是___________。
(4)尾气中主要含有___________,还含有少量的PH3、H2S和HF等.将尾气先通入纯碱溶液,可除去___________;再通入次氯酸钠溶液,可除去___________(均填化学式)。
(5)相比于湿法磷酸,热法磷酸工艺复杂,能耗高,但优点是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了证明在实验室制备得到的Cl2中会混有HCl,甲同学设计了如图所示的实验装置,按要求回答下列问题。
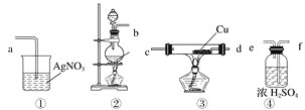
(1)请根据甲同学的示意图,所需实验装置从左至右的连接顺序:装置②→__________。
(2)装置②中主要玻璃仪器的名称__________、__________、__________。
(3)实验室制备Cl2的离子方程式为____________。
(4)装置③中Cu的作用__________(用化学方程式表示)。
(5)乙同学认为甲同学实验设计仍然存在缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为此,乙同学提出气体通入装置①之前,要加装一个检验装置⑤,以证明最终通入AgNO3溶液中的气体只有一种。你认为装置⑤应放入__________。
(6)丙同学看到甲同学设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成紫色石蕊试液,如果观察到__________的现象,则证明制Cl2时有HCl挥发出来。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有MgCl2和Al2(SO4)3的混合溶液,向其中不断加入NaOH溶液,得到的沉淀量与加入的NaOH溶液的体积关系如图所示,则原溶液中MgCl2和Al2(SO4)3的物质的量浓度之比为( )

A. 1:2 B. 2:1 C. 1:1 D. 2:3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2 L容器中三种物质的物质的量随时间的变化曲线如图所示。由图中数据分析,该反应的化学方程式和反应开始至2 min末Z的平均反应速率分别为( )
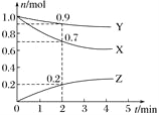
A. X+3Y![]() 2Z 0.1 mol/(L·min) B. 2X+Y
2Z 0.1 mol/(L·min) B. 2X+Y![]() 2Z 0.1 mol/(L·min)
2Z 0.1 mol/(L·min)
C. X+2Y![]() Z 0.05 mol/(L·min) D. 3X+Y
Z 0.05 mol/(L·min) D. 3X+Y![]() 2Z 0.05 mol/(L·min)
2Z 0.05 mol/(L·min)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为2 L的密闭容器中进行如下反应:A(g)+2B(g)![]() 3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
3C(g)+nD(g),开始时A为4 mol,B为6 mol;5 min后达到化学平衡,此时C的物质的量为3 mol,用D表示的化学反应速率v(D)为0.2 mol·L-1 min-1。
(1)5 min末B的物质的量浓度为________。
(2)前5 min内化学反应速率v(A)为_______。
(3)化学方程式中n值为________。
(4)该反应在此温度下的平衡常数K=______(填数值)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X为一种常见酸的浓溶液,能使蔗糖粉末变黑。A与X反应的转化关系如下图所示,其中反应条件及部分产物均已略去,则下列有关说法正确的是( )
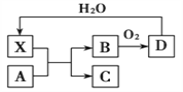
A. X使蔗糖变黑的现象主要体现了X的强氧化性
B. 若A为铁,则足量A与X在室温下即可完全反应
C. 若A为碳单质,则将C通入少量的澄清石灰水,一定可以观察到白色沉淀产生
D. 工业上,B转化为D的反应条件为高温、常压、使用催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁、移动支付、共享单车、网购,被称为中国“新四大发明”。用于高铁和共享单车制造业的重要金属材料是( )

A.Na﹣K合金B.Cu﹣Sn合金C.Sn﹣Pb合金D.Mg﹣Al合金
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com