
| A、向同浓度的Na2CrO4和NaCl混合溶液中滴加AgNO3溶液,AgCl先析出 | ||||
| B、向AgCl饱和溶液中加入NaCl晶体,有AgCl析出且溶液中 c(Ag+)=c(Cl-) | ||||
C、AgCl和Ag2CrO4共存的悬浊液中,
| ||||
| D、向Ag2CrO4的悬浊液中加入NaCl浓溶液,Ag2CrO4不可能转化为AgCl |
| Ksp(AgCl) |
| c(Cl-) |
|
| c(Cl-) |
| c(CrO42-) |
| ||
|
| Ksp(AgCl)?c(Ag+) |
| Ksp(CrO42-) |


科目:高中化学 来源: 题型:
| A、(NH4)2SO4溶于水:(NH4)2SO4═2NH4++SO42- |
| B、H3PO4溶于水:H3PO4═3H++PO43- |
| C、HF溶于水:HF?H++F- |
| D、NaHS溶于水:NaHS═Na++HS-,HS-?H++S2- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1:1 |
| B、1:2:3 |
| C、6:3:2 |
| D、3:2:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
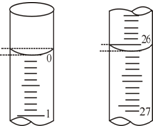 为测定某品牌洗厕精的酸(盐酸)含量,某学生欲用已知物质的量浓度的NaOH溶液来测定该洗厕精(盐酸)的物质的量浓度时,选择酚酞作指示剂.请填写下列空白:
为测定某品牌洗厕精的酸(盐酸)含量,某学生欲用已知物质的量浓度的NaOH溶液来测定该洗厕精(盐酸)的物质的量浓度时,选择酚酞作指示剂.请填写下列空白:| 滴定次数 | 待测盐酸的体积/mL | 0.1000mol/LNaOH溶液的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 2.00 | 28.15 | 26.15 |
| 第二次 | 25.00 | 1.50 | 29.50 | 28.00 |
| 第三次 | 25.00 | 0.20 | 26.55 | 26.35 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量稀硫酸中和冲洗 |
| C、配制硫酸溶液时,可先在量筒中加入一定量的水,再在搅拌下慢慢加入浓硫酸 |
| D、鉴别食盐和芒硝晶体,可用口尝药品的味道,有咸味者,则为食盐晶体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com