
下列叙述中,正确的是( )
A.甲烷的标准燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+ 2O2 (g)=CO2(g)+2H2O(g) △H=-890.3 kJ·mol-1
B.500℃、30MPa下,将0.5 molN2和1.5molH2置于密闭的容器中充分反应生成NH3(g),放热193kJ,其热化学方程式为:N2+3H2 2NH3(g) △H=-38.6kJ·mol-1
2NH3(g) △H=-38.6kJ·mol-1
C.活化能的作用在于使反应物活化,所以化学反应的活化能不可能接近于零或等于零
D.常温下,反应C(s)+ CO2 (g)=2CO(g)不能自发进行,则该反应的△H>0
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案科目:高中化学 来源:2017届辽宁省铁岭市高三上学期第一次联考化学试卷(解析版) 题型:选择题
相对分子质量为M的气态化合物VL(已换算成标准状况)溶于m g水中,得到溶液的溶质质量分数为ω%,物质的量浓度为c mol/L,密度为ρg•cm-3,则下列说法正确的是( )
A.相对分子质量M可表示为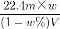
B.物质的量浓度C可表示为: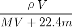
C.溶液的质量分数ω可表示为: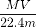
D.溶液密度p可表示为: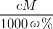
查看答案和解析>>
科目:高中化学 来源:2017届江苏省苏州市高三上学期期初调研化学试卷(解析版) 题型:选择题
一定温度下,在三个体积均为2.0 L的恒容密闭容器中发生如下反应:PCl5(g) PCl3(g)+Cl2(g)
PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始物质的量 (mol) | 平衡物质的量 (mol) | 达到平衡所需时间 (s) | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
下列说法正确的是
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ<容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=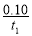 mol·L-1·s-1
mol·L-1·s-1
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl3 0.45 mol和Cl2 0.10 mol,则反应将向逆反应方向进行
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.21周考化学卷(解析版) 题型:计算题
已知反应FeO(s)+CO(g)  Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
Fe(s)+CO2(g) 的Kc=0.5(1273K)。若起始浓度c(CO)=0.05 mol·L-1,c(CO2)=0.01 mol·L-1,请回答:
(1)判断化学反应进行的方向并计算反应物、生成物的平衡浓度。
(2)CO的转化率是多少?
(3)增加FeO的量,对平衡有无影响?
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.21周考化学卷(解析版) 题型:选择题
下列说法中正确的是( )
A.8NH3(g)+6NO2(g)=7N2(g)+12H2O(g);△H<0 ,则该反应一定能自发进行
B.提取海带中碘元素时,为将I-完全氧化为I2,用HNO3作氧化剂比用H2O2效果好
C.原电池放电过程中,负极质量一定减轻,正极的质量一定增加
D.由于Ksp( MgCO3)< Ksp[Mg(OH)2],因此水垢中MgCO3会逐渐转化为Mg(OH)2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上9.21周考化学卷(解析版) 题型:选择题
下列有关说法错误的是( )
A.为保护海轮的船壳,常在船壳上镶入锌块
B.纯碱溶于热水中,去污效果增强,说明纯碱的水解反应是吸热反应
C.已知工业合成氨气△H<0,达平衡后,升高温度,正反应速率减小,逆反应速率增大,平衡向逆反应方向移动
D.NH3(g)+ HCl(g)= NH4Cl(s)较低温度下能自发进行,说明该反应的△H<0
查看答案和解析>>
科目:高中化学 来源:2017届四川省、温江中学等五校高三上第一次联考化学卷(解析版) 题型:填空题
元素铬(Cr)在溶液中主要以Cr3+(蓝紫色)、Cr(OH)4?(绿色)、Cr2O72?(橙红色)、CrO42?(黄色)等形式存在,Cr(OH)3为难溶于水的灰蓝色固体,回答下列问题:
(1)Cr3+与Al3+的化学性质相似。在Cr2(SO4)3溶液中逐滴加入NaOH溶液直至过量,可观察到的现象是____ _____。
(2)CrO42?和Cr2O72?在溶液中可相互转化。室温下,初始浓度为1.0 mol·L?1的Na2CrO4溶液中c(Cr2O72?)随c(H+)的变化如图所示。
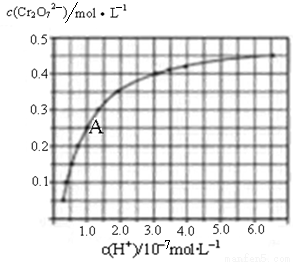
①用离子方程式表示Na2CrO4溶液中的转化反应 。
②由图可知,溶液酸性增大,CrO42?的平衡转化率__________(填“增大”“减小”或“不变”)。根据A点数据,计算出该转化反应的平衡常数为__________。
③升高温度,溶液中CrO42?的平衡转化率减小,则该反应的ΔH________0(填“大于”“小于”或“等于”)。
(3)在化学分析中采用K2CrO4为指示剂,以AgNO3标准溶液滴定溶液中Cl?,利用Ag+与CrO42?生成砖红色沉淀,指示到达滴定终点。当溶液中Cl?恰好沉淀完全(浓度等于1.0×10?5 mol·L?1)时,溶液中c(Ag+)为_______ mol·L?1,此时溶液中c(CrO42?)等于__________ mol·L?1。(已知Ag2CrO4、AgCl的Ksp分别为2.0×10?12和2.0×10?10)。
(4)+6价铬的化合物毒性较大,常用NaHSO3将废液中的Cr2O72?还原成Cr3+,该反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2017届四川省、温江中学等五校高三上第一次联考化学卷(解析版) 题型:选择题
下列化工生产过程中,未涉及氧化还原反应的是
A.海带提碘 B.氯碱工业 C.氨碱法制纯碱 D.海水提溴
查看答案和解析>>
科目:高中化学 来源:2017届山东省淄博市高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A.氢氧燃料电池工作时,1mol H2在正极上失去2mol电子
B.0.1mol/LNa2CO3溶液加热后,溶液的CO32-的数目小于6.02×1022个
C.常温常压下,22.4LCl2中含有的分子数为6.02×1023个
D.室温下,稀释0.1mol/LCH3COOH溶液,溶液的导电能力减弱
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com