

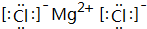 ,故答案为:
,故答案为: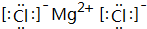 ;
;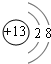 ,故答案为:
,故答案为: ;
;

 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:
| A、15mL | B、25mL |
| C、35mL | D、50mL |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有较多Fe3+的溶液:Na+、SO42-、HS-、NH4+ |
| B、c(OH-)=1mol/L的溶液:AlO2-、CH3COO-、K+、Ba2+ |
| C、pH=1的溶液:K+、Fe2+、NO3-、Na+ |
| D、遇Al能放出H2的溶液:HCO3-、K+、Mg2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学反应原理在工业生产中具有十分重要的意义.
化学反应原理在工业生产中具有十分重要的意义.| 温度/℃ | 500 | 700 | 900 |
| K | 1.00 | 1.47 | 2.40 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 为研究HA、HB溶液和MOH的酸碱性的相对强弱,某化学学习小组设计了以下实验:室温下,将pH=2的两种酸溶液HA、HB和pH=12的碱溶液MOH各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图所示,根据所给数据,请回答下列问题:
为研究HA、HB溶液和MOH的酸碱性的相对强弱,某化学学习小组设计了以下实验:室温下,将pH=2的两种酸溶液HA、HB和pH=12的碱溶液MOH各1mL,分别加水稀释到1000mL,其pH的变化与溶液体积的关系如图所示,根据所给数据,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
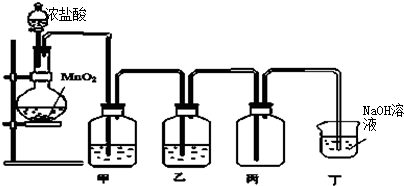
查看答案和解析>>
科目:高中化学 来源: 题型:
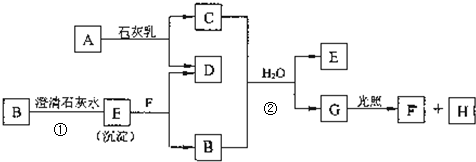
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 六种一溴二甲苯的熔点 | 234℃ | 206℃ | 213.8℃ | 204℃ | 214.5℃ | 205 |
| 对应还原二甲苯的熔点 | -13℃ | -54℃ | -27℃ | -54℃ | -27℃ | -54℃ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com