
在密闭容器中进行如下反应:X2(g)+Y2(g)  2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
2Z(g),已知X2、Y2、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到平衡时,各物质的浓度有可能是
A.Z为0.3mol/L B.Y2为0.4mol/L
C.X2为0.2mol/L D.Z为0.4mol/L
科目:高中化学 来源:2015-2016学年河北省高二上第一次月考化学试卷(解析版) 题型:选择题
在某温度时,pH=3的某水溶液中c(OH-)=10-9 mol·L-1,现有该温度下的四份溶液:①pH=2的CH3COOH;②0.01 mol·L-1的HCl;③pH=11的氨水;④pH=11的NaOH溶液。下列说法正确的是
A.①中水的电离程度最小,③中水的电离程度最大
B.若将②与④按照10∶1的体积比混合,混合溶液的pH﹤7
C.将四份溶液稀释相同倍数后,溶液的pH:③>④>②>①
D.将四份溶液稀释相同倍数后,溶液的pH:④>③>①>②
查看答案和解析>>
科目:高中化学 来源:2016届江苏省高三上学期10月月考化学试卷(解析版) 题型:实验题
某课外活动小组设计了以下实验验证Ag与浓硝酸反应的过程中可能产生NO。其实验流程图如下:

(1)测定硝酸的物质的量反应结束后,从如图装置B中所得100 mL溶液中取出25.00 mL溶液,用0.1 mol·L-1的NaOH溶液滴定,用酚酞作指示剂,滴定前后的滴定管中液面的位置如上图所示。在B容器中生成硝酸的物质的量为______ mol,则Ag与浓硝酸反应过程中生成的NO2在标准状况下的体积为___________mL。

(2)测定NO的体积
①从如图所示的装置中,你认为应选用________装置进行Ag与浓硝酸反应实验,选用的理由是_______。
②选用如图所示仪器组合一套可用来测定生成NO体积的装置,其合理的连接顺序是__________(填各导管口编号)。
③在测定NO的体积时,若量筒中水的液面比集气瓶的液面要低,此时应将量筒的位置_______(填“下降”或“升高”),以保证量筒中的液面与集气瓶中的液面持平。
(3)气体成分分析
若实验测得NO的体积为112.0 mL(已折算到标准状况),则Ag与浓硝酸反应的过程中______(填“有”或“没有”)NO产生,作此判断的依据是_________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年吉林省高二下期末化学试卷(解析版) 题型:填空题
(1~5小题每空2分,6小题3分,共17分)
以下是实验室常用的部分仪器,请回答下列问题


(1)序号为⑥和⑩的仪器的名称分别为________、________。
(2)在过滤操作中,必须用到上述仪器中的___(填序号),次外,上图中还缺少的玻璃仪器 (填名称)。
(3)能作反应容器且可直接加热的仪器是上述中的________(填名称)。
(4)仪器上标有温度的是_______(填序号)。
(5)如图是温度计、量筒、滴定管的一部分,下述读数(虚线刻度)及说法正确的是

A.①是量筒,读数为2.5 mL
B.②是量筒,读数为2.5 mL
C.③是滴定管,读数为2.5 mL
D.②是温度计,读数是2.5 ℃
(6)丙同学想用如图装置以大理石和稀盐酸反应制取CO2。教师指出,这需要太多的稀盐酸,造成浪费。该同学选用了上述①~⑩中的一种仪器,加在装置上,解决了这个问题。请你把该仪器画在图中合适的位置 。
。

查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二9月月考化学试卷(解析版) 题型:选择题
X、Y、Z三种气体,把a mol X与b mol Y充入一密闭容器中,发生反应X+2Y 2Z.达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为
2Z.达到平衡时,若它们的物质的量满足:n(X)+n(Y)=n(Z),则Y的转化率为
A.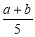 ×100% B.
×100% B.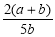 ×100%
×100%
C. ×100% D.
×100% D.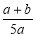 ×100%
×100%
查看答案和解析>>
科目:高中化学 来源:2016届浙江省富阳市高三上学期第二次质量检测化学试卷(解析版) 题型:选择题
化学是人类创造新物质的工具。下列各种物质的现代工业生产原理或过程的描述与事实不相符的是
A.用电解法制取Na、Mg、Al
B.电解熔融NaCl制Cl2
C.以硫或硫铁矿为原料通过接触法制硫酸
D.制硅:
查看答案和解析>>
科目:高中化学 来源:2016届江西省九江市七校高三第一次联考化学试卷(解析版) 题型:选择题
设NA表示阿伏加德罗常数的数值,下列说法正确的是
A.1mol/L的Ca(ClO)2溶液中含ClO-数目为2NA
B.标准状况下,22.4 L三氯甲烷的原子数约为4 NA个
C.体积分别为1.0L pH==2的盐酸与硫酸溶液中氢离子数均为0.01NA
D.1 mol —OH与1 molOH-所含电子数均为9 NA
查看答案和解析>>
科目:高中化学 来源:2016届福建省福州市高三上学期第二次质量检测考试化学试卷(解析版) 题型:实验题
(16分)辉铜矿(主要成分为Cu2S)经火法冶炼,可制得Cu和H2SO4,流程如下图所示:
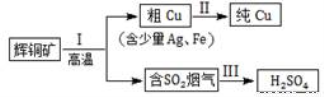
(1) Cu2S中Cu元素的化合价是 价。
(2)Ⅱ中,电解法精炼粗铜(含少量Ag、Fe),CuSO4溶液做电解质溶液:
①粗铜应与直流电源的 极(填“正”或“负”)相连。
②铜在阴极析出,而铁以离子形式留在电解质溶液里的原因是 。
③电解一段时间后,溶液中Cu2+浓度 (填“减小”、“增大”、“不变”)。
(3)Ⅲ中,烟气(主要含SO2、CO2)在较高温度经下图所示方法脱除SO2,并制得H2SO4。
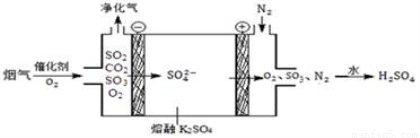
① 在阴极放电的物质是___________。
② 在阳极生成SO3的电极反应式是____________。
(4)检测烟气中SO2脱除率的步骤如下:
i.将一定量的净化气(不含SO3)通入足量NaOH溶液后,再加入足量溴水。
ii.加入浓盐酸,加热溶液至无色无气泡,再加入足量BaCl2溶液。
iii.过滤、洗涤、干燥,称量沉淀质量。
①用离子方程式表示i中溴水的主要作用____________。
②若沉淀的质量越大,说明SO2的脱除率越____________(填“高”或“低”)。
(5)次磷酸(H3PO2)是一种精细磷化工产品,具有较强还原性。H3PO2是一元中强酸,写出其电离方程式 ·
③NaH2PO2为_ (填“正盐”或“酸式盐”)其溶液显 (填“弱酸性”、“中性”或“弱碱性”)。
查看答案和解析>>
科目:高中化学 来源:2016届河北省高三上学期二调化学试卷(解析版) 题型:选择题
在一定温度下,某浓度的硝酸与金属锌反应生成N02和NO,两者的物质的量之比为1:3,则要使1mol金属锌完全反应,反应过程中消耗此硝酸的物质的量为
A.2.4 mol B.2.6 mol C.2.8mol D.3.2 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com