
| A.新制氯水中所含分子只有Cl2和H2O分子,所含的离子只有H+、Cl-、ClO-和OH- |
| B.新制氯水能杀菌消毒是因为Cl2有毒,能毒杀细菌 |
| C.氯水光照条件下有气泡逸出,该气体是Cl2 |
| D.氯水放置数天后酸性会增强 |
 培优三好生系列答案
培优三好生系列答案 优化作业上海科技文献出版社系列答案
优化作业上海科技文献出版社系列答案科目:高中化学 来源:不详 题型:填空题
 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CuSO4溶液不能产生丁达尔现象,Fe(OH)3胶体能产生丁达尔现象 |
| B.向石蕊试液中加入新制氯水,石蕊试液变红后一直保持 |
| C.向淀粉KI溶液中滴加少量新制氯水,溶液变蓝色 |
| D.在新制氯水和久置氯水中滴加AgNO3溶液都有白色沉淀生成 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题

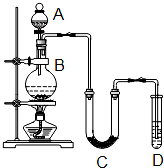
| 实验步骤 | 预期现象和结论 |
| 步骤1:取适量洗气瓶B中溶液于试管A中,滴加______. | 若产生的白色沉淀,则洗气瓶B溶液中存在SO42-. |
| 步骤2:另取适量洗气瓶B中溶液于试管B中,滴加______. | 产生白色沉淀. |
| 步骤3:取步骤2后试管B中的上层清液于试管C中,滴加______. | ______ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com