
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A.0.5 mol O3与11.2 L O2所含的分子数一定相等
B.常温常压下,78 g Na2O2和Na2S的混合物中含有的阴离子数为NA
C.2SO2(g)+O2(g)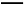 2SO3(g)和SO2(g)+
2SO3(g)和SO2(g)+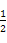 O2(g)
O2(g)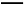 SO3(g)的ΔH相等
SO3(g)的ΔH相等
D.物质的量浓度为0.25 mol/L的MgCl2溶液中,含有Cl-个数为0.5NA
科目:高中化学 来源:2014高考化学名师选择题专练 电解质溶液练习卷(解析版) 题型:选择题
下列溶液中有关微粒的物质的量浓度或物理量关系正确的是( )
A.NaHSO3和NaHCO3的中性混合溶液中(S和C均用R表示):c(Na+)=c(HR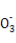 )+2c(R
)+2c(R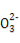 )
)
B.常温下将醋酸钠、盐酸两溶液混合后,溶液呈中性,则混合后溶液中:c(Na+)>c(Cl-)>c(CH3COOH)
C.常温下物质的量浓度相等的①(NH4)2CO3、②(NH4)2SO4、③(NH4)2Fe(SO4)2三种溶液中c(N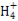 ):①<③<②
):①<③<②
D.等体积等物质的量浓度的NaClO溶液与NaCl溶液中离子总数:N前>N后
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学反应中的能量变化练习卷(解析版) 题型:选择题
将洁净的金属片甲、乙、丙、丁分别放置在浸有某种盐溶液的滤纸上并压紧(如图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下表(已知构成两电极的金属其金属活泼性相差越大,电压表的读数越大:
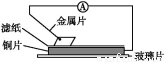
金属 | 电子流动方向 | 电压/V |
甲 | 甲→Cu | +0.78 |
乙 | Cu→乙 | -0.25 |
丙 | 丙→Cu | +1.35 |
丁 | 丁→Cu | +0.30 |
依据记录数据判断,下列结论中正确的是( )
A.将甲、乙形成的合金露置在空气中,甲先被腐蚀
B.金属乙能从硫酸铜溶液中置换出铜
C.在四种金属中丙的还原性最弱
D.甲、丁若形成原电池时,甲为正极
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 化学与STSE练习卷(解析版) 题型:选择题
化学与科学、技术、社会、环境密切相关。下列有关说法中错误的是( )
A.推广使用风能、太阳能等新能源能够减少温室气体的排放
B.餐桌上的瓷盘是硅酸盐制品
C.制作航天服的聚酯纤维和用于光缆通信的光导纤维都是新型无机非金属材料
D.用“84”消毒液来杀死H1N1流感病毒是因为病毒蛋白质变性
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 元素周期表元素周期律练习卷(解析版) 题型:选择题
如图是部分短周期元素原子半径与原子序数的关系图,下列说法不正确的是( )
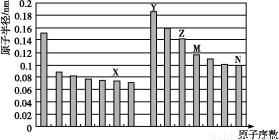
A.N、Z两种元素的离子半径相比前者较大
B.M、N两种元素的气态氢化物的稳定性相比后者较强
C.X与M两种元素组成的化合物能与碱反应,但不能与任何酸反应
D.工业上常用电解Y和N形成的化合物的熔融态制取Y的单质
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 NA的应用练习卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值,若等质量的H2O和D2O分别与一定质量的金属钾完全反应,转移的电子数均为 NA,则下列各量不相等的是( )
NA,则下列各量不相等的是( )
A.消耗H2O和D2O的物质的量
B.同温同压下生成气体的体积
C.反应后所得溶液中溶质的质量分数
D.参加反应的钾的质量
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 物质结构与性质练习卷(解析版) 题型:填空题
(1)已知X、Y、Z为第三周期元素,其原子的第一至第四电离能如下表:
电离能/kJ·mol-1 | I1 | I2 | I3 | I4 |
X | 578 | 1 817 | 2 745 | 11 578 |
Y | 738 | 1 451 | 7 733 | 10 540 |
Z | 496 | 4 562 | 6 912 | 9 543 |
则X、Y、Z的电负性从大到小的顺序为 (用元素符号表示),元素Y的第一电离能大于X的第一电离能的原因是
。
(2)A、B、C、D是周期表中前10号元素,它们的原子半径依次减小。D能分别与A、B、C形成电子总数相等的分子M、N、W,且在M、N、W分子中,A、B、C三原子都采取sp3杂化。
①A、B、C的第一电离能由小到大的顺序为 (用元素符号表示)。
②M是含有 键的 分子(填“极性”或“非极性”)。
③N是一种易液化的气体,请简述其易液化的原因:
。
④W分子的VSEPR模型的空间构型为 ,W分子的空间构型为 。
⑤AB-中和B2分子的π键数目比为 。
(3)E、F、G三元素的原子序数依次增大,三原子的核外的最外层电子排布均为4s1。
①E元素组成的单质的晶体堆积模型为 (填字母)。
a.简单立方堆积b.体心立方堆积
c.六方最密堆积d.面心立方最密堆积
②F元素在其化合物中最高化合价为 。
③G2+的核外电子排布式为 ,G2+和N分子形成的配离子的结构式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师综合题专练 有机合成与推断练习卷(解析版) 题型:填空题
已知:Ⅲ能与NaHCO3溶液反应,Ⅲ和Ⅳ的相对分子质量相等且Ⅳ催化氧化的产物不能发生银镜反应。
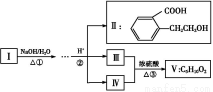
(1)化合物Ⅲ中官能团的名称是 ;Ⅱ不能发生的反应是 。
A.加成反应B.消去反应
C.酯化反应D.水解反应
(2)反应③的类型为 。
(3)Ⅴ的结构简式为 ,Ⅰ的结构简式为 。
(4)化合物Ⅵ是Ⅱ的同分异构体,同时符合下列四种条件,则Ⅵ的结构简式为 。
A.苯环上有两个取代基且苯环上的一氯代物有2种
B.能与FeCl3溶液发生显色反应
C.能发生水解反应
D.核磁共振氢谱有6个峰,峰的面积之比为1∶2∶2∶2∶2∶1
(5)化合物Ⅱ发生分子内成环反应的化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师知识点精编 专题9溶液中的电离平衡练习卷(解析版) 题型:填空题
25 ℃时,电离平衡常数:
弱酸的化学式 | CH3COOH | HClO | H2CO3 |
电离平衡常数(25 ℃) | 1.8×10-5 | 3.0× | K1=4.3×10-7 K2=5.6×10-11 |
回答下列问题:
(1)物质的量浓度为0.1 mol/L的下列四种物质:
a.Na2CO3,b.NaClO,c.CH3COONa,d.NaHCO3;
pH由大到小的顺序是 (填编号)。
(2)常温下0.1 mol/L的CH3COOH溶液加水稀释过程中,下列表达式的数据一定变小的是 ;
A.c(H+) B.c(H+)/c(CH3COOH) C.c(H+)·c(OH-) D.c(OH-)/c(H+)
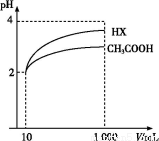
(3)体积为10 mL pH=2的醋酸溶液与一元酸HX分别加水稀释至1 000 mL,稀释过程pH变化如图,则HX的电离平衡常数 (填“大于”、“等于”或“小于”)醋酸的平衡常数;理由是 ,
稀释后,HX溶液中水电离出来的c(H+) (填“大于”、“等于”或“小于”)醋酸溶液中水电离出来的c(H+),理由是 ;
(4)25 ℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中c(CH3COO-)-c(Na+)= (填准确数值)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com