
| A. | 称取8.0gCuSO4,加入500mL水 | |
| B. | 称取7.68gCuSO4,加入480mL水 | |
| C. | 称取12.5gCuSO4•5H2O,加水配成500mL溶液 | |
| D. | 称取12.0gCuSO4•5H2O,加水配成480mL溶液 |
分析 配制480mL溶液,需要选用500mL容量瓶,需要硫酸铜物质的量为:0.1mol/L×0.5L=0.05mol,需要硫酸铜的质量为:160g/mol×0.05mol=8.0g,需要胆矾的质量为:250g/mol×0.05mol=12.5g,根据以上计算进行解答.
解答 解:实验室需用480mL 0.1mol•L-1 CuSO4溶液,实际上配制的是500mL 0.1mol/L的硫酸铜溶液,需要硫酸铜的质量为8.0g,需要胆矾的质量为12.5g,
A.称取8.0gCuSO4,加入500mL水,则溶液的体积大于500mL,故A错误;
B.需要配置的是500mL溶液,故应将8.0gCuSO4溶于水使溶液的体积为500mL,而不是加入到480mL水中,故B错误;
C.需要胆矾的质量为12.5g,且胆矾溶于水中,使所配溶液体积是500mL,故C正确;
D.需要配置的是500mL溶液,故应将12.50g胆矾溶于水使溶液的体积为500mL,而不是将12.0g胆矾加入到480mL水中,故D错误.
故选C.
点评 本题考查了配制一定物质的量浓度的溶液方法,题目难度不大,注意掌握配制一定浓度溶液的方法,熟悉实验室中容量瓶的规格,试题培养了学生灵活应用所学知识的能力.


科目:高中化学 来源: 题型:解答题
 已知H2O(g)=H2(g)+$\frac{1}{2}$O2(g),反应过程中能量变化如图所示.请回答下列问题:
已知H2O(g)=H2(g)+$\frac{1}{2}$O2(g),反应过程中能量变化如图所示.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在加热条件下,浓硫酸和浓硝酸均能与木炭反应 | |
| B. | 将浓硫酸和浓硝酸分别长期露置于空气中,浓度均会升高 | |
| C. | 稀硫酸和稀硝酸分别与金属反应时,S和N元素的化合价都会发生变化 | |
| D. | 因为浓硫酸和浓硝酸都能与铝反应,所以常温下二者都不能用铝制容器盛放 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙醇与金属钠反应 | B. | 苯和液溴反应生成溴苯 | ||
| C. | 乙烯和溴的四氯化碳溶液反应 | D. | 乙酸和乙醇反应生成乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图:
在一容积为2L的密闭容器内加入0.2mol的N2和0.6mol的H2,在一定条件下发生如下反应:N2(g)+3H2(g)?2NH3(g)△H<0反应中NH3的物质的量浓度的变化的情况如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

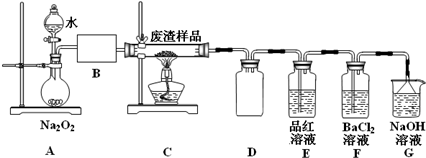
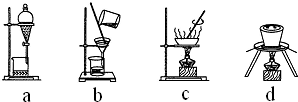
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.90 | 20.02 | 19.98 | 20.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氮氧化物是形成光化学烟雾和酸雨的一个重要原因 | |
| B. | 玻璃钢是钢与玻璃纤维形成的复合材料 | |
| C. | 石油化工废弃物易造成水体富营养化 | |
| D. | 硫酸铵是常用的一种硝态氮肥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com