
【题目】I.将少量饱和氯化铁溶液滴入沸水中,继续煮沸,可制得Fe(OH)3胶体,反应的方程式为: 。
。
①当溶液呈________时,停止加热,即制得Fe(OH)3胶体。
②氢氧化铁胶体粒子直径大小的范围是____________________。
③下列叙述错误的是________。(单选)
A. 雾属于胶体,能产生丁达尔效应
B. “PM 2.5”悬浮在空气中形成胶体,危害人体健康 (“PM 2.5”指大气中直径小于或等于2.5微米的细小颗粒物,也可称为可吸入肺颗粒物)
C. 明矾、硫酸铁可以净水,净水原理和胶体有关
D. 胶体在一定条件下能稳定存在,属于介稳体系
Ⅱ.(1)下列4组物质均有一种物质的类别与其它3种不同
A. CaO、Na2O、CO2、CuO B. H2、C、P、Cu
C. O2、Fe、Cu、Zn D. HCl、H2O、H2SO4、HNO3
以上四组物质中与别不同的物质依次是(填化学式):
A________________;B________________;C________________;D________________。
(2)请对以下过程形成的分散系进行分类
①花生油加入到水中后充分搅拌; ②向蒸馏水中加入硝酸钾至恰好饱和;
③将饱和氯化铁溶液逐滴加入沸水中,继续加热,直至出现红褐色;
④澄清石灰水中通入少量的CO2; ⑤水和酒精的混合物;
属于浊液的是:________(填序号,下同);属于溶液的是:________。
(3)下列物质:①HCl ②蔗糖 ③NaOH ④KCl ⑤SO2 ⑥Fe ⑦碳酸钠溶液
属于电解质的是:___________(填序号),属于非电解质的是:___________(填序号),能导电的是:_____________________(填序号)。
【答案】红褐色 1~100 nm B CO2 Cu O2 H2O ①④ ②⑤ ①③④ ②⑤ ⑥⑦
【解析】
I.①制备氢氧化铁胶体,可将饱和氯化铁滴加到沸水中,并加热至溶液呈红褐色;
②胶体分散质粒子的直径在1nm~100nm之间;
③A.雾分散质粒子直径在1nm~100nm之间;
B.胶体的微粒直径在1-100nm之间;
C.明矾净水是水解生成氢氧化铝胶体净水;硫酸铁是水解生成氢氧化铁胶体净水;
D.胶体是介稳分散系。
Ⅱ.(1)根据物质的组成和性质进行分类;
(2)分散系可以根据分散质微粒直径的大小,分为浊液、胶体、溶液
(3)在水溶液或者熔融状态下,能导电的化合物为电解质;在水溶液或者熔融状态下,不能导电的化合物为非电解质;只要有自由移动的带电微粒就可以导电。
I. ①实验室制备氢氧化铁胶体是在沸腾的蒸馏水中加入饱和氯化铁溶液,当溶液变为红褐色时立即停止加热;
②胶体分散质粒子的直径在1nm~100nm之间;
③A.雾分散质粒子直径在1nm~100nm之间,属于胶体,能产生丁达尔效应,故不选A;
B.“ “PM2.5”指大气中直径小于或等于2.5微米的细小颗粒物,直径大于100nm,在空气中形不成胶体,故选B;
C.明矾净水是水解生成氢氧化铝胶体净水;硫酸铁是水解生成氢氧化铁胶体净水;
,故不选C;
D.胶体在一定条件下能稳定存在,属于介稳体系,故不选D;
答案:B
Ⅱ.(1)A. CaO、Na2O、CuO为金属氧化物,CO2为非金属氧化物;
B.H2、C、P为非金属单质,Cu为金属单质;
C.Fe、Cu、Zn为金属单质,O2为非金属单质;
D.HCl、H2SO4、HNO3为酸,H2O不属于酸;
(2)①花生油加入到水中后充分搅拌,花生油难溶于水,形成乳浊液;
②向蒸馏水中加入硝酸钾至恰好饱和,形成溶液;
③将饱和氯化铁溶液逐滴加入沸水中,继续加热,直至出现红褐色,生成氢氧化铁胶体;
④澄清石灰水中通入少量的CO2,生成碳酸钙沉淀和水,属于悬浊液;
⑤水和酒精互溶,构成溶液;
(3)在水溶液或者熔融状态下,能导电的化合物为电解质,常见的电解质有酸、碱、盐、水,活泼金属的氧化物和过氧化物等,符合条件的有①③④;
在水溶液或者熔融状态下,不能导电的化合物为非电解质,符合条件的有②⑤;
只要有自由移动的带电微粒就可以导电,符合条件的有⑥⑦。


科目:高中化学 来源: 题型:
【题目】无水FeCl2易吸湿、易被氧化,常作为超高压润滑油的成分。某实验小组利用无水FeCl3和氯苯(无色液体,沸点132.2℃)制备少量无水FeCl2,并测定无水FeCl2的产率。
实验原理:2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑
实验装置:按如图所示组装好的装置,检查气密性后,向三颈烧瓶A中加入16.76g无水FeCl3和22.5g氯苯。
回答下列问题:

(1)利用工业氮气(含有H2O、O2、CO2)制取纯净干燥的氮气。
①请从下列装置中选择必要的装置,确定其合理的连接顺序:a→________→上图中的j口(按气流方向,用小写字母表示)。

②实验完成后通入氮气的主要目的是________。
(2)装置C中的试剂是________(填试剂名称),其作用是________。
(3)启动搅拌器,在约126℃条件下剧烈搅拌30min,物料变成黑色泥状。加热装置A最好选用__(填字母)。
a.酒精灯 b.水浴锅 c.电磁炉 d.油浴锅
(4)继续升温,在128~139℃条件下加热2h,混合物颜色逐渐变浅,黏度降低。该步骤中加热温度已经接近或超过氯苯沸点,但氯苯实际损失量却非常小,其原因是________。
(5)继续加热1h后放置冷却,在隔绝空气条件下过滤出固体,用洗涤剂多次洗涤所得固体,置于真空中干燥,得到成品。若D中所得溶液恰好与25mL2.0mol·L-1NaOH溶液完全反应,则该实验中FeCl2的产率约为________(保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤素及其化合物广泛存在于自然界中。回答下列问题:
(1)光气(COCl2)是一种重要的有机中间体,在农药、医药、工程塑料、聚氨酯材料以及军事上都有许多用途。光气的分子立体构型为______________,其三种元素的电负性由小到大的顺序为______________。与COCl2互为等电子体的分子和离子(各写一种)__________。
(2)日常生活中,看到的许多可见光,如霓虹灯,试从原子结构角度解释这一现象?____________________________。
(3)区分晶态二氧化硅和非晶态二氧化硅最可靠的科学方法是_____________。
(4)一种铜的溴化物晶胞结构如图所示,若将图中的Cu去掉,再把所有的Br换成Cu,得到晶体铜的晶胞结构,则晶体铜的堆积方式为___________,某同学将基态铜原子价电子错误的写为3d94s2,违背了核外电子排布规律中的______。
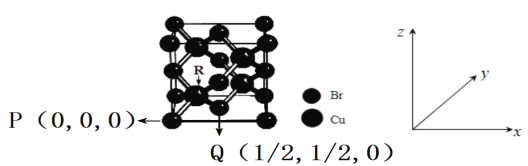
(5)下列关于上述铜的溴化物晶胞结构说法正确的是_________(选填字母序号)。
A.该化合物的化学式为CuBr2
B.铜的配位数为8
C.与每个Br紧邻的Br有12个
D.由图中P点和Q点的原子坐标参数,确定R点的原子坐标参数为(1/4,1/4,1/4)
(6)若图中P点和R点的原子核间距为a cm,NA为阿伏伽德罗常数的值,则该晶胞密度为______g/cm3。(列出计算式即可)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列反应中,水既不是氧化剂,也不是还原剂的是
A.2Na+2H20=2Na0H+H2↑ B.C12+H20=HC1+HC10
C.2F2+2H20=4HF+02 D.2H20![]() 2H2↑+02↑
2H2↑+02↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在一定容积的密闭容器中加入NH3和O2各1mol,发生反应:4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
4NO(g)+6H2O(g)。下列说法中,表明该反应达到化学平衡状态的是
A. NO和H2O浓度比不再变化 B. v(NH3)正=v(NH3)逆
C. 气体的密度不再变化 D. v(NH3)正=v(O2)逆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】勒夏特列原理是自然界一条重要的基本原理,下列事实能用勒夏特列原理解释的是
A. NO2气体受压缩后,颜色先变深后变浅
B. 对2HI(g) ![]() H2(g)+I2(g)平衡体系加压,颜色迅速变深
H2(g)+I2(g)平衡体系加压,颜色迅速变深
C. 合成氨工业采用高温、高压工艺提高氨的产率
D. 配制硫酸亚铁溶液时,常加入少量铁屑以防止氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组的同学进行三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O分解的实验探究。经小组讨论,他们设计了如下装置进行实验。烧瓶B中盛有饱和NH4Cl和饱和NaNO2混合液(常用于实验室制N2),干燥管C1中装有碱石灰。

(1)B中发生反应的化学方程式为______________________________________。
(2)C2的作用是_________________,C3中盛装的试剂是___________________。
(3)若实验中观察到E1、E4中的澄清石灰水均变浑浊,则E3中的现象是___________________,证明气体产物是___________________。
(4)实验装置中有2个酒精灯,先点燃A1,一段时间后,熄灭A1,关闭活塞a,再点燃A2,待D中的样品充分反应后,再次打开活塞a,点燃A1,则第二次点燃A1的理由是________________________________________________________。
(5)该小组同学查阅资料后推知, D中固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。实验测得C2、C3共增重5.4g;将D中固体生成物溶于水,测得最后残余固体的质量为6.88g。通过计算,固体产物中铁元素的存在形式为______(需表示出产物的物质的量)。
若要通过实验研究上述结论,除3%H2O2、蒸馏水外,还需要下列试剂中的___________。
A.1.0 mol·L-1HNO3 B.1.0 mol·L-1盐酸 C.1.0 mol·L-1NaOH溶液
D.0.1 mol·L-1KI溶液 E.0.1 mol·L-1CuSO4溶液 F.20%KSCN溶液。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有含NaCl、Na2SO4和NaNO3的混合物,选择适当的试剂将其转化为相应的沉淀或固体,从而实现Cl-、SO42-、和NO3-的相互分离。相应的实验过程可用下图表示:

请回答下列问题:
(1)写出实验流程中下列物质的化学式:
试剂X :______________ 沉淀A:______________ 沉淀B:________________。
(2)上述实验流程中加入过量的Na2CO3的目的是____________________________。
(3)按此实验方案得到的溶液3中肯定含有__________(填化学式)杂质。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com