
 2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )
2 NH3 (g); △H <0, 该反应应采取的适宜条件是( )| A.低温、高压、催化剂 | B.适宜的温度、高压、催化剂 |
| C.低温、常压、催化剂 | D.适宜的温度和压强、催化剂 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.硫铁矿燃烧前需将矿粒粉碎,这样易于向沸腾炉中投料 |
| B.炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应 |
| C.SO2氧化为SO3时需使用催化剂,这样可提高SO2的转化率 |
| D.接触室的反应温度控制在400~500 ℃,因为在该温度范围内催化剂的活性较高 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.使用太阳能等代替化石燃料,符合低碳节能减排的要求 |
| B.油脂在碱性条件下水解可制得肥皂 |
| C.海轮外壳上镶入锌块,可减缓船体的腐蚀 |
| D.二氧化硫的大量排放是造成光化学烟雾的主要原因 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.硝酸钾 | B.碳酸钾 | C.硫酸钾 | D.氯化钾[ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
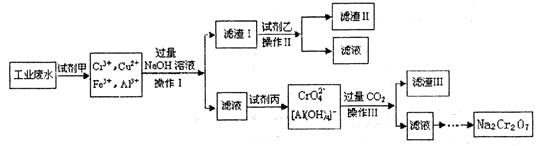
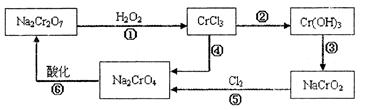
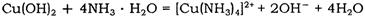
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.合成氨工业用铁触媒作催化剂,可加快正、逆反应速率 |
| B.合成氨工业对原料气进行压缩,可增大原料气的转化率 |
| C.硫酸工业中,采取通入适当过量的空气,以提高SO2的转化率 |
| D.硫酸工业中,在催化反应室安装热交换装置可利用SO3转化为H2SO4时放出的热量 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
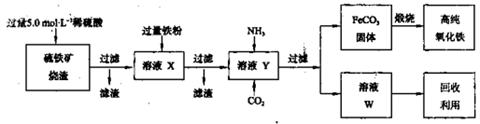
 (1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式: 。
(1)上述实验所涉及的反应中,有一个反应既属于化合反应,又属于氧化还原反应。写出该反应的离子方程式: 。
| A.MnO2与浓盐酸反应制备Cl2 |
| B.Cu与浓硫酸反应生成SO2 |
| C.由KMnO4分解制O2 |
| D.乙醇与乙酸反应制备乙酸乙酯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com