
| A. | 80% | B. | 75% | C. | 60% | D. | 40% |
分析 一定条件下将0.5mol SO2和一定量O2通入恒容密闭容器中,压强为4.04×105Pa,在恒温(500℃)下反应达到平衡,压强为3.03×105Pa,测得余0.1mol O2,依据化学平衡三段式列式计算,设起始量氧气物质的量为x
2SO2+O2=2SO3
起始量(mol) 0.5 x 0
变化量(mol) 2(x-0.1)x-0.1 2(x-0.1)
平衡量(mol)0.5-2(x-0.1)0.1 2(x-0.1)
压强之比等于气体物质的量之比计算得到x,转化率=$\frac{消耗量}{起始量}$×100%.
解答 解:依据化学平衡三段式列式计算,设起始量氧气物质的量为x
2SO2+O2=2SO3
起始量(mol) 0.5 x 0
变化量(mol) 2(x-0.1)x-0.1 2(x-0.1)
平衡量(mol)0.5-2(x-0.1)0.1 2(x-0.1)
压强之比等于气体物质的量之比计算得到x,
$\frac{0.5-2(x-0.1)+0.1+2(x-0.1)}{0.5+x}$=$\frac{3.03×1{0}^{5}}{4.04×1{0}^{5}}$
x=0.3mol
转化率=$\frac{消耗量}{起始量}$×100%=$\frac{0.5-2(0.3-0.1)}{0.5}$×100%=80%,
故选A.
点评 本题考查了化学平衡的计算分析应用,主要是平衡三段式的计算方法,气体相同条件下压强之比等于气体物质的量之比,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | CH2=CH-CH=CH2 1,3二丁烯 | B. | 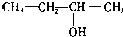 3-丁醇 | ||
| C. | 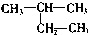 2-甲基丁烷 2-甲基丁烷 | D. | 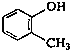 甲基苯酚 甲基苯酚 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.03mol/L HA与0.03mol/L NaA等体积混合得到的碱性溶液中:c(Na+)>c(A--) | |
| B. | 酸性溶液中水的电离程度一定比纯水的电离程度小 | |
| C. | pH相等的CH3COONa、NaOH和Na2CO3三种溶液c(NaOH)<c(CH3COONa<c((Na2CO3 | |
| D. | 室温下,pH=3的CH3COOH溶液和pH=11的NaOH溶液等体积混合后,pH大于7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学键 | Si-O | Si-Cl | H-H | H-Cl | Si-Si | Si-C |
| 键能/kJ•mol-1 | 460 | 360 | 436 | 431 | 176 | 347 |
| A. | 236 kJ•mol-1 | B. | -116 kJ•mol-1 | C. | -236 kJ•mol-1 | D. | 116 kJ•mol-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用稀硫酸除去铜绿:4H++Cu2(OH)2CO3═2Cu2++CO2↑+3H2O | |
| B. | Fe3O4与稀硝酸反应的离子方程式为:Fe3O4+8H+═Fe2++2Fe3++4H2O | |
| C. | 向NH4Al(SO4)2溶液中滴入Ba(OH)2溶液恰好使SO42-完全沉淀:2Ba2++NH4++Al3++2SO42-+4OH-═Al(OH)3↓+NH3•H2O+2BaSO4↓ | |
| D. | 少量氢氧化钙溶液与碳酸氢钠溶液混合:Ca2++2OH-+2HCO3-═CaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
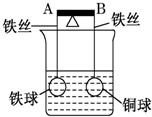 如图杠杆AB两端分别挂着体积相同质量相同的空心铁球和空心铜球.调节杠杆使其保持平衡,一段时间后小心加入浓CuSO4溶液,回答下列有关问题(不考虑铁丝反应和两球的浮力变化)
如图杠杆AB两端分别挂着体积相同质量相同的空心铁球和空心铜球.调节杠杆使其保持平衡,一段时间后小心加入浓CuSO4溶液,回答下列有关问题(不考虑铁丝反应和两球的浮力变化)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com