
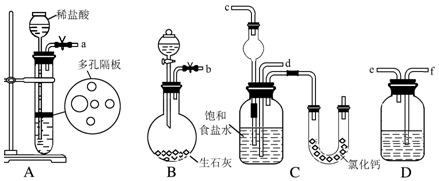
分析 (1)根据装置A制取CO2,装置B制取NH3,装置D除去二氧化碳中的HCl,二氧化碳与氨气通入C中,其中氨气应防止倒吸,据此分析连接仪器装置;
(2)A装置是制备二氧化碳气体一般用碳酸钙和盐酸反应生成,二氧化碳气体中含有氯化氢气体,会影响碳酸氢钠的生成,D为装置除杂可以用饱和碳酸氢钠溶液;
(3)氨气易溶于水,二氧化碳在水中的溶解度较小,制取碳酸氢钠时先要得到含氨的饱和食盐水;
(4)C中用球形干燥管球形部分空间大,液面上升缓慢,起缓冲作用,所以不用直导管;装有无水CaCl2的U形管的作用吸收多余的NH3;
(5)分离NaHCO3固体通常用过滤操作;
(6)为了析出氯化铵晶体,则向滤液中加入适量的NaCl粉末,提高氯离子浓度,使NH4Cl晶体析出;实验证明所得固体的成分大部分是氯化铵,是利用氯化铵的性质,受热生成氯化氢和氨气气体,在试管口处温度降低重新生成固体氯化铵分析判断.
解答 解:(1)向饱和氯化钠溶液中通入足量的二氧化碳与氨气反应生成NaHCO3沉淀,则装置A产生CO2,装置B产生NH3,装置D除去二氧化碳中的HCl,二氧化碳与氨气通入C中,其中氨气应防止倒吸,则b接c,故a接f、e接d,
故答案为:f、e、d、c;
(2)A装置是制备二氧化碳气体的反应,所以固体为CaCO3用块状石灰石,生成的二氧化碳气体中含有氯化氢,若不除去碳酸氢钠难以形成,所以应用饱和碳酸氢钠溶液或饱和氯化钠溶液除去,故答案为:块状石灰石;饱和NaHCO3溶液;
(3)候氏制碱方法是利用氨气溶解性大极易溶解于水,二氧化碳气体水中溶解性较小,实验饱和食盐水中先通入氨气,再通入二氧化碳气体;实验操作过程中,应让B装置先发生反应,
故答案为:B;
(4)氨气极易溶于水,用直导管向饱和氯化钠溶液中通入氨气,容易发生倒吸,C中用球形干燥管球形部分液面上升慢起缓冲作用,可以防止倒吸;装有无水CaCl2的U形管的作用吸收多余的NH3,故答案为:防倒吸;吸收多余的NH3;
(5)分离NaHCO3固体和液体用过滤的方法,故答案为:过滤;
(6)第四步中为了析出氯化铵晶体,则向滤液中加入适量的NaCl粉末,提高氯离子浓度,使NH4Cl晶体析出;所得的氯化铵晶体中常含有少量的氯化钠和碳酸氢钠(约占5%~8%),设计简单的实验证明所得固体的成分大部分是氯化铵,是利用氯化铵的分解产物为气体,温度降低氨气和氯化氢气体会重新生成固体氯化氨,方法为:取少量样品于试管中,用酒精灯加热,看到试管上端有白烟生成(或试管口有白色晶体),最后剩余极少量的固体,从而证明所得固体的成分大部分是氯化铵;
故答案为:NaCl;取少量样品于试管中,用酒精灯加热,看到试管上端有白烟生成(或试管口有白色晶体),最后剩余极少量的固体,从而证明所得固体的成分大部分是氯化铵.
点评 本题考查了实验制备碳酸氢钠的过程分析和装置作用判断,掌握候氏制碱的反应原理和反应特征是解题关键,熟练掌握工业制备流程和注意问题,能顺利解决问题,侧重于考查学生的实验探究能力,题目难度中等.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2gH2中含有的分子数为NA | |
| B. | 1mol Zn变成Zn2+时失去的电子数为NA | |
| C. | 1L1mol•L-1MgCl2溶液中含有的Cl-数为NA | |
| D. | 常温常压下,22.4LO2含有的原子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 营养液所含成分 | 质量(g) |
| KCl | a |
| K2SO | b |
| NH4Cl | 428 |
| A. | 53.5 和214 | B. | 74.5 和348 | C. | 74.5 和696 | D. | 149 和696 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
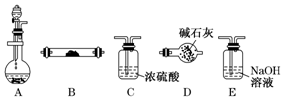 如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.
如图是用于气体制备、干燥、性质验证、尾气处理的部分仪器装置(加热及夹持固定装置均已略去).请根据下列要求回答问题.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
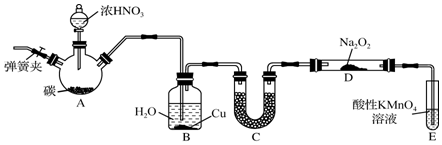
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
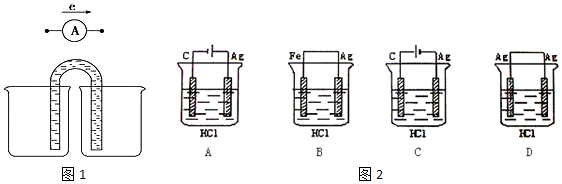
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com