
只用一种试剂就可以鉴别乙酸溶液、葡萄糖溶液、蔗糖溶液,这种试剂是
A.NaOH溶液 B.Cu(OH)2悬浊液 C.石蕊试液 D.Na2CO3溶液
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源:2013-2014湖南省衡南县高二下学期期末考试化学试卷(解析版) 题型:选择题
进行化学实验、观察实验现象,通过分析、推理得出正确的结论是化学学习的方法之一。下列对有关实验事实的解释正确的是( )
A.将N2和过量的O2在高温或放电的条件下反应得到红棕色的气体,说明NO为红棕色气体
B.用干净的铂丝蘸取少量溶液在酒精灯外焰上灼烧,发现火焰呈黄色,则溶液中含Na+
C.在AgNO3的溶液中加入锌粉,能置换出银,说明Ag+的还原性比Zn2+强
D.浓硫酸放入蔗糖中,能使蔗糖炭化,说明浓硫酸具有吸水性
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省衡南县高一下学期期末考试化学试卷(解析版) 题型:选择题
下列各项中表达正确的是( )
A.F原子结构示意图: 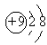 B.H2O的电子式:
B.H2O的电子式:
C.1H、2H、3H是三种不同元素 D.乙烯的分子式: C2H4
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省益阳市高二上学期期末考试化学试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值。下列有关叙述正确的是( )
A.50℃时,pH=l的1.0 L H2SO4溶液中含有的H+数目为0.1NA
B.1 molC5H12分子中共价键总数为14NA
C.室温下,21.0g乙烯和丁烯的混合气体中含有的氢原子数目为1.5NA
D.高温下,60g SiO2与足量纯碱反应,最多可释放出2NA气体分子
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省益阳市高一上学期期末考试化学(理)试卷(解析版) 题型:实验题
硫代硫酸钠与稀硫酸的反应为:Na2S2O3+H2SO4=Na2SO4+S↓+SO2↑+H2O。某实验兴趣小组用如下图所示的实验装置探究外界条件对化学反应速率的影响(加热仪器和夹持仪器均已省略)
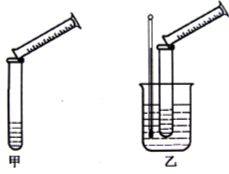
(1)实验目的:
装置甲,探究浓度对化学反应速率的影响;装置乙,探究 对化学反应速率的影响。
(2)装置乙中的加热方法称为 加热,该加热方法具有 、
等优点。
(3)通过甲、乙装置,分别进行了四组实验,数据记录如下,并经分析得出相关结论:
实验组号 | 温度 | Na2S2O3 | H2SO4 | 加入H2O 的体积 | 出现沉淀 所需时间 | ||
体积 | 浓度 | 体积 | 浓度 | ||||
Ⅰ | 0OC | 5mL | 0.1mol/L | 10mL | 0.1mol/L | 5mL | 8s |
Ⅱ | 0OC | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 12s |
Ⅲ | 30OC | 5mL | 0.1mol/L | 5mL | 0.1mol/L | 10mL | 4s |
Ⅳ | 30OC | 5mL | 0.2mol/L | 5mL | 0.2mol/L | 10mL | 2s |
结论1: ;
结论2: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省益阳市高一上学期期末考试化学(理)试卷(解析版) 题型:选择题
蓄电池在放电时起原电池作用,在充电时起电解池作用。下面是爱迪生蓄电池分别在充电和放电时发生的反应:Fe+NiO2+2H2O Fe(OH)2+Ni(OH)2。下列有关爱迪生蓄电池的说法正确的是
Fe(OH)2+Ni(OH)2。下列有关爱迪生蓄电池的说法正确的是
A.放电时,Fe是负极,发生还原反应,NiO2是正极,发生氧化反应
B.蓄电池的电极可以浸入某种酸性电解质溶液中
C.放电时,电解质溶液中的阴离子向正极方向移动
D.充电时,阴极上的电极反应式为:Fe(OH)2+2e-=Fe+2OH-
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省益阳市高一上学期期末考试化学(理)试卷(解析版) 题型:选择题
NA代表阿伏加德罗常数的数值。下列有关叙述正确的是( )
A.标准状况下,22.4L水中含有的分子数为NA
B.11.2LNH3中所含的质子数为5NA
C.常温常压下,48gO3含有的氧原子数为3NA
D.2.4g 金属镁变为镁离子时失去的电子数为0.1NA
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省怀化市高三第三次模拟考试理综化学试卷(解析版) 题型:填空题
金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀等性质被广泛用在高新科技材料和航天领域中。“硫酸法”生产钛的原料是钛铁矿(主要成分是:FeTiO3,还含有少量Mn、Zn、Cr、Cu等重金属元素及脉石等杂质);主要生产流程如下:
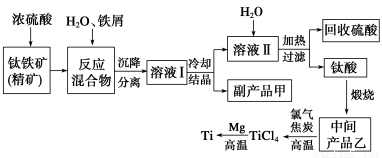
已知反应:①将钛铁矿与浓H2SO4煮【解析】
FeTiO3+2H2SO4(浓)△TiOSO4(硫酸氧钛)+FeSO4+2H2O。②加水热分解硫酸氧钛:TiOSO4+(n+1)H2O△TiO2·nH2O+H2SO4。
请回答下列问题:
(1)副产品甲是____________,可循环利用的物质是___________________________。
(2)上述生产流程中加入铁屑的目的是_______________________________________。
(3)写出中间产品乙与焦炭、氯气在高温下发生反应的方程式为:________________。
(4)“硫酸法”生产钛排放的废液对水体有哪些污染,请指出主要的两点:
①_________________________________;②_______________________________。
针对其中一项污染,提出处理的方法: 。
查看答案和解析>>
科目:高中化学 来源:2013-2014湖南省五市十校高一下学期期中教学质量检测化学试卷(解析版) 题型:选择题
关于如图所示装置的叙述,正确的是
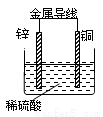
A.锌是正极,铜片上有气泡产生
B.铜片质量逐渐减少
C.电流从锌片经导线流向铜片
D.氢离子在铜片表面被还原
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com